老化遺伝子で読み解くロンジェビティ──健康長寿時代の新常識

私たちはなぜ老いるのでしょうか。
この問いは、古くから哲学や宗教のテーマであり続けてきましたが、現代ではついに「分子レベル」で答えが見え始めています。
その中心にあるのが「遺伝子」です。
私たちの体は約2万個の遺伝子によって設計されていますが、その中には「老化のスピード」を調整するものが確かに存在します。
かつて老化は避けられない運命でした。
しかし今、医学はそれを「調整可能なプロセス」として捉え始めています。
本コラムでは、老化遺伝子という視点から、抗老化医学がどこまで進んでいるのかを、初心者にもわかりやすく、かつ専門的な視点も交えながら解き明かしていきます。
「老化遺伝子」と「長寿遺伝子」とは
─ 寿命を動かすアクセルとブレーキ
まず理解すべきは、老化は単純な「劣化」ではないという点です。
むしろ、遺伝子によって制御された“プログラムの一部”と考えられています。
私たちの体には、「寿命制御遺伝子」と呼ばれる仕組みが存在します。
これは、車でいうアクセルとブレーキのような関係で成り立っています。
老化遺伝子は、本来は細胞を修復し、異常を防ぐ「メンテナンス担当」です。しかし、この機能が低下すると、結果的に老化が加速します。
つまり「壊れて老化する」のではなく、「修復できなくなって老化する」のです。
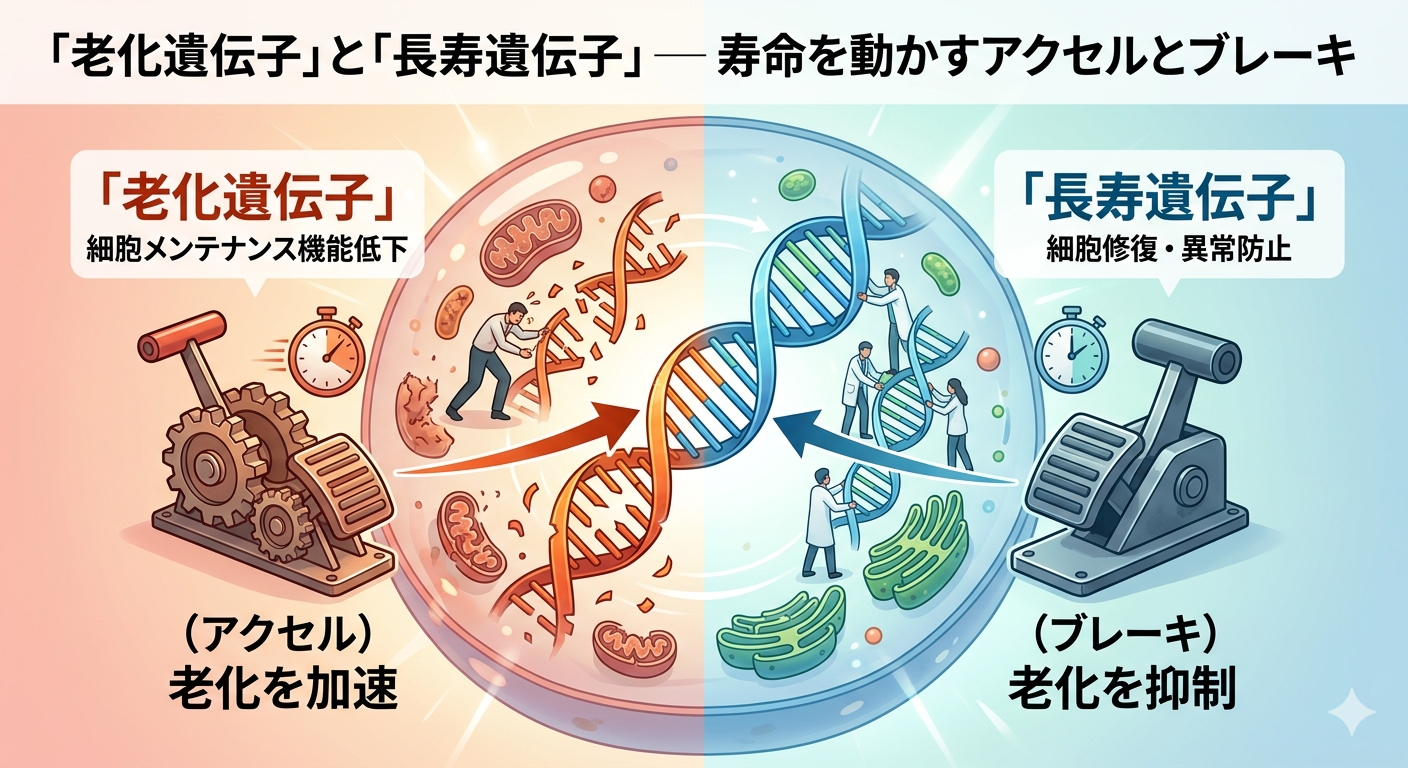
一方で、サーチュイン(SIRT1〜7)に代表される長寿遺伝子は、代謝やDNA修復、炎症制御を担う「ブレーキ役」として働きます。
興味深いことに、これらはカロリー制限や運動、さらには特定の栄養素(例:レスベラトロール)によって活性化されることが知られています。
つまり私たちは、遺伝子に支配されているだけでなく、ある程度“操作できる側”にもいるのです。
参考記事:レスベラトロールとロンジェビティ──サーチュインと代謝制御から考える抗老化実践
早老症研究が教えてくれた「DNAの番人」
─ 老化は“設計図の崩れ”から始まる
老化遺伝子の存在が明らかになった最大のきっかけは、「早老症」の研究でした。これは、実年齢よりも何倍ものスピードで老化が進行する疾患です。こうした病気を調べることで、老化の仕組みそのものが見えてきました。
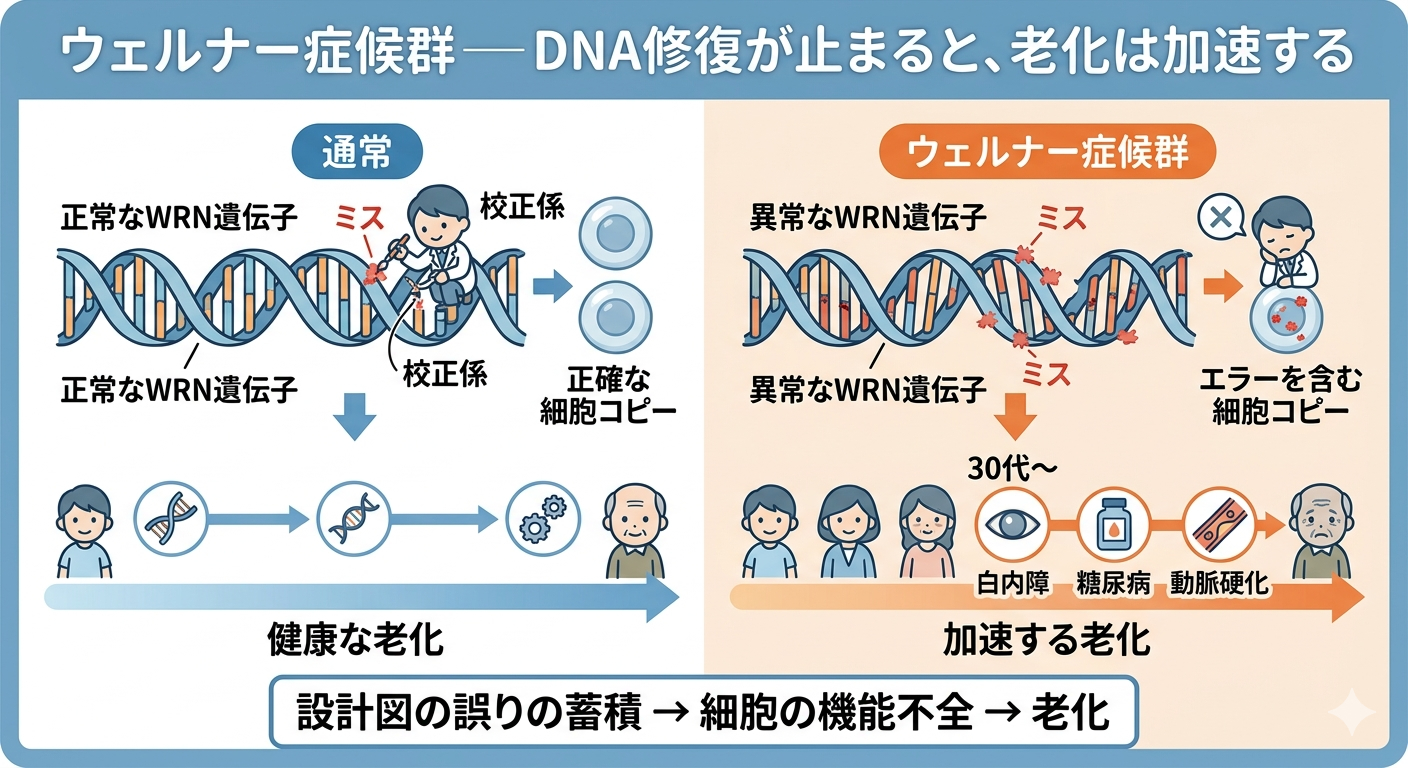
ウェルナー症候群
─ DNA修復が止まると、老化は加速する
代表的な早老症の一つがウェルナー症候群です。患者さんでは、30代頃から白内障や糖尿病、動脈硬化といった高齢者に多い病気が現れます。
この原因は、WRNというDNA修復遺伝子の異常です。DNAは日々コピーされ続けていますが、その過程では小さなミスが必ず起こります。WRNは、その誤りを見つけて直す「校正係」のような存在です。
もしこの校正係がいなければ、設計図の誤りは少しずつ蓄積し、細胞は次第に機能不全を起こします。これが、老化の本質的な一側面だと考えられています。
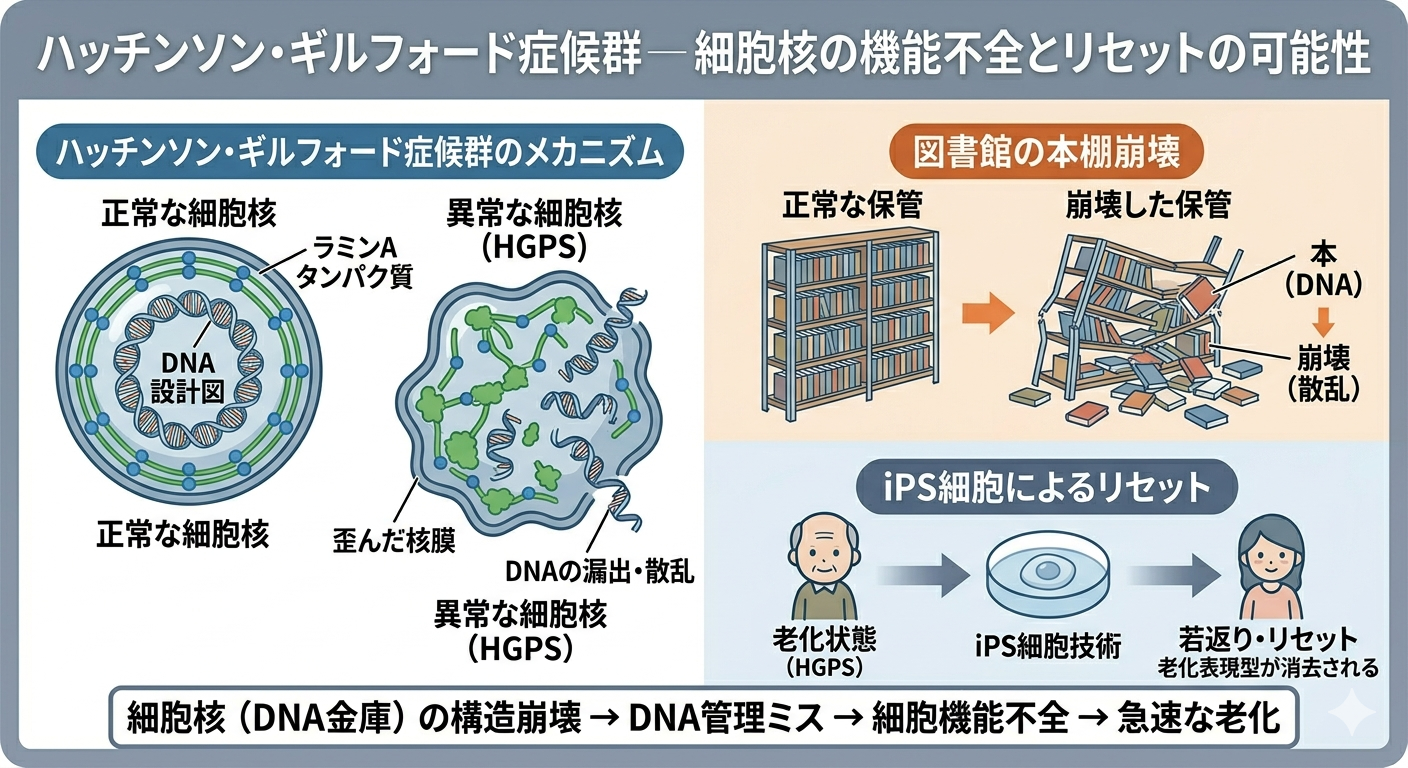
ハッチンソン・ギルフォード症候群
─ 細胞核という“金庫”が壊れる病気
さらに重篤な早老症として知られるのが、ハッチンソン・ギルフォード症候群です。こちらは小児期から急速な老化症状が進行する疾患で、原因は核膜タンパク質ラミンAの異常にあります。
細胞核は、大切なDNAを保管する“設計図の金庫”のような場所です。ラミンAは、その金庫の壁や骨組みを支える重要な部材です。
この構造が壊れると、核の形は歪み、DNAが外に漏れ出すような異常な状態になります。例えるなら、図書館の本棚が崩れ、本が散乱してしまっている状態です。
設計図を正しく保管できなければ、細胞が正常に働けなくなるのは当然です。
近年ではiPS細胞技術により、この異常な老化表現型がリセットされることも確認されており、「老化は巻き戻せる可能性がある」という新たな視点も生まれています。
モデルマウスが示した「老化の正体」
─ 時間・代謝・酸化という三つの軸
老化は、見た目の変化だけではありません。細胞の内部では、時間とともに少しずつ機能低下が進み、やがて組織や臓器全体の衰えとして現れます。こうした複雑な現象を科学的に理解するために、大きな役割を果たしてきたのが「モデルマウス研究」です。
特定の遺伝子を欠損させたり、逆に強く働かせたりしたマウスを観察することで、老化の原因がより明確になってきました。中でも重要なのが、「時間」「代謝」「酸化」という三つの軸です。
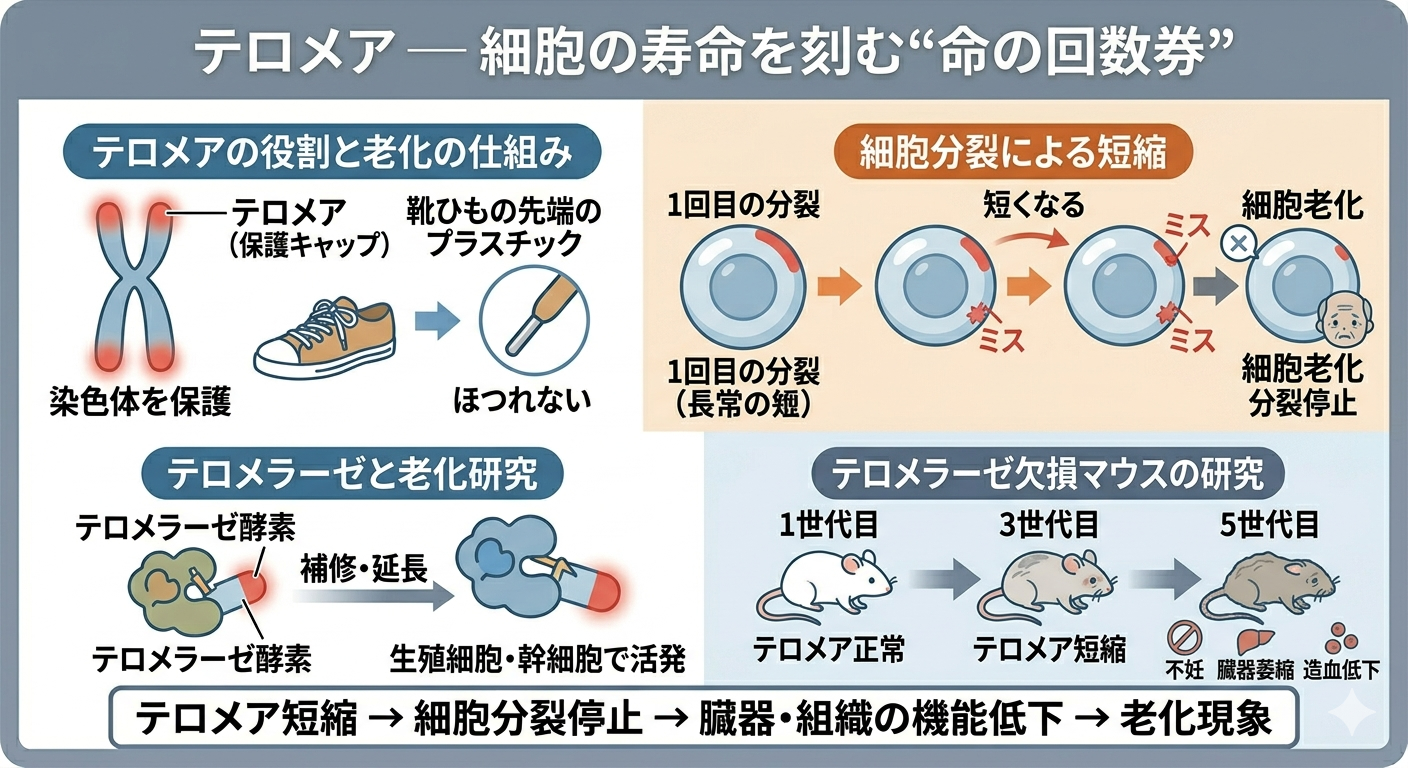
テロメア
─ 細胞の寿命を刻む“命の回数券”
私たちの細胞は、無限に分裂できるわけではありません。細胞分裂には回数制限があり、そのカギを握るのが「テロメア」です。
テロメアは染色体の末端にある保護キャップのような構造で、靴ひもの先端に付いているプラスチック部分をイメージするとわかりやすいでしょう。
あの部分があるからこそ、ひもはほどけません。同じように、テロメアは染色体の端を守り、遺伝情報が壊れないように保護しています。
しかし細胞が一度分裂するたびに、このテロメアは少しずつ短くなっていきます。やがて一定の長さを下回ると、細胞はそれ以上分裂できなくなり、「細胞老化」という状態に入ります。これは細胞が寿命を迎えたサインです。
テロメラーゼという酵素は、この短くなったテロメアを補修する働きを持っています。生殖細胞や幹細胞では比較的活発ですが、一般的な体細胞ではその働きは限定的です。
テロメラーゼを欠損させたマウスでは、世代を重ねるごとにテロメアが短縮し、不妊、臓器萎縮、造血機能低下など、典型的な老化現象が現れます。
これは、老化が単なる年齢ではなく、「細胞分裂の履歴」によっても進行することを示しています。
つまりテロメアは、体内に存在する“見えない寿命カウンター”なのです。
参考記事:テロメアとは何か?健康長寿のカギを握る“命の回数券”の正体
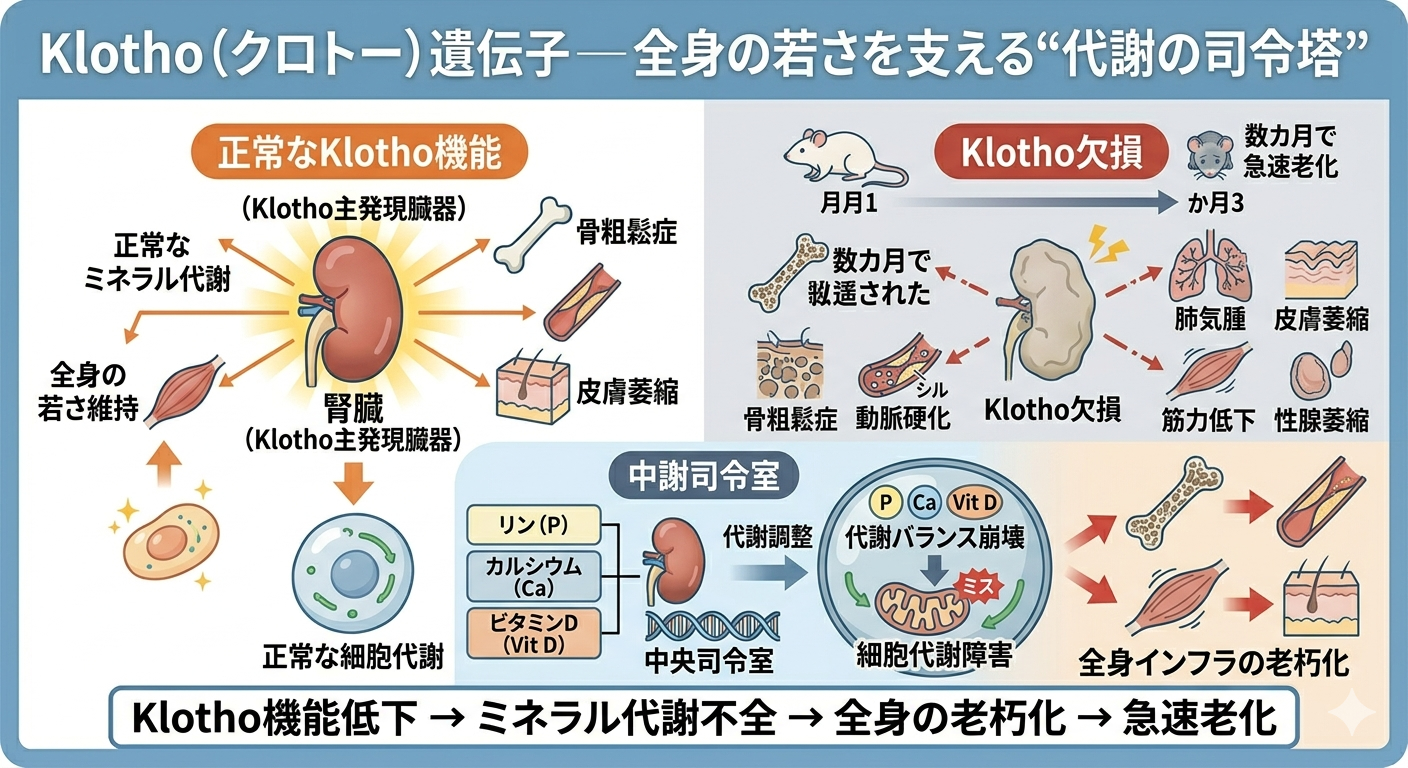
Klotho(クロトー)遺伝子
─ 全身の若さを支える“代謝の司令塔”
Klotho遺伝子は、老化研究において非常に象徴的な存在です。なぜなら、この遺伝子が働かないマウスは、わずか数カ月で急速な老化症状を示すからです。
Klotho欠損マウスでは、動脈硬化、骨粗鬆症、皮膚萎縮、肺気腫、筋力低下、性腺萎縮など、多臓器にわたる老化現象が短期間で進行します。まるで時間が何倍もの速度で流れているかのような状態です。
この遺伝子は主に腎臓で強く発現し、リン・カルシウム・ビタミンDなどのミネラル代謝を調整しています。言い換えれば、体内の資源配分を管理する“中央司令室”のような存在です。
もしこの司令塔が機能しなければどうなるか。血管にはカルシウムが沈着し、骨は逆にもろくなり、細胞の代謝バランスも崩れます。結果として、全身のインフラが同時多発的に老朽化していくのです。
近年では、人間でもKlothoレベルが高い人ほど認知機能や腎機能、血管年齢との関連が良好である可能性が報告され、注目を集めています。
Klothoは、単なる長寿遺伝子ではなく、「全身の若さを保つ調整因子」と考えられています。
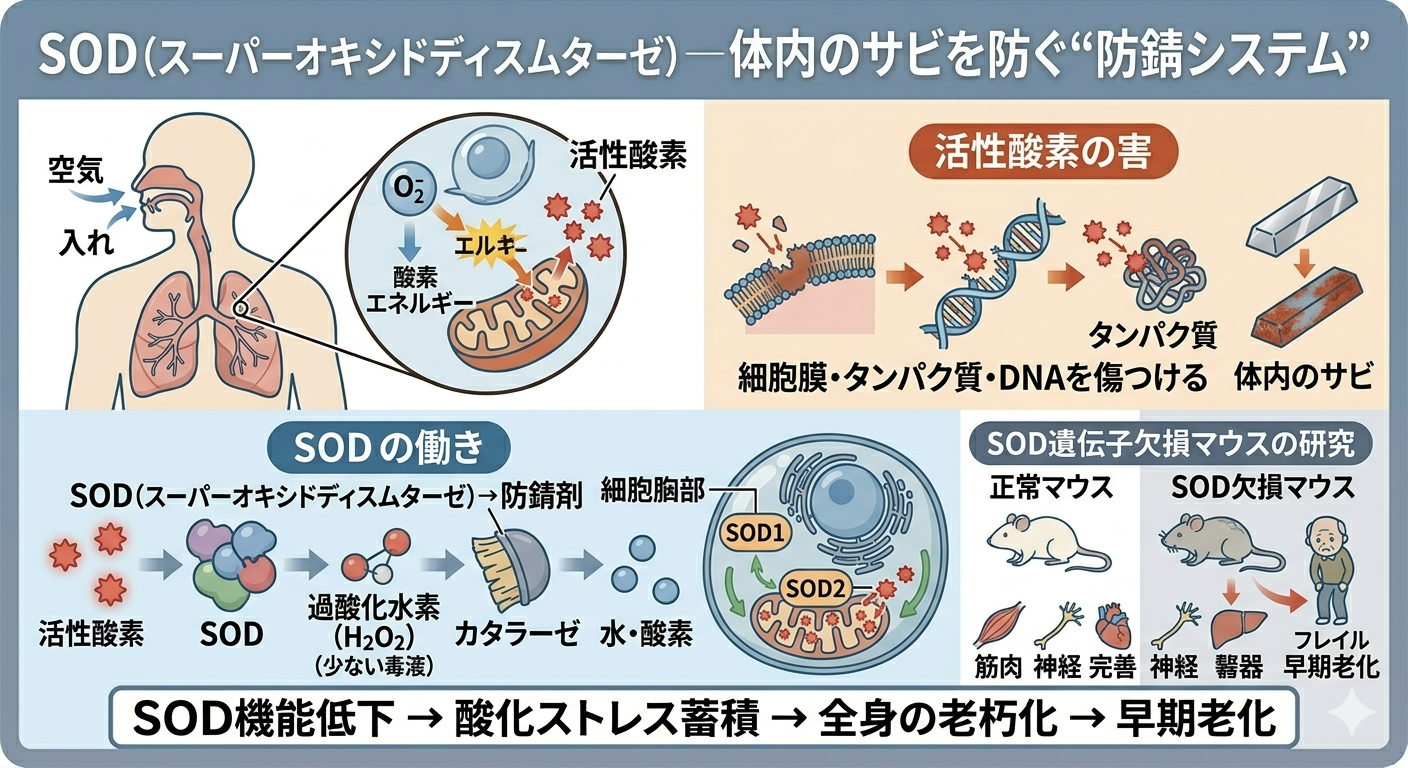
SOD(スーパーオキシドディスムターゼ)
─ 体内のサビを防ぐ“防錆システム”
私たちは呼吸をして生きていますが、その呼吸の過程では必ず「活性酸素」が生まれます。
活性酸素は細菌やウイルスを排除する役割もありますが、過剰になると細胞膜、タンパク質、DNAを傷つける危険な存在になります。
これは金属が酸化してサビる現象に近く、体内ではこのダメージが老化の一因になります。
そこで働くのが、SOD(スーパーオキシドディスムターゼ)です。SODは活性酸素の一種であるスーパーオキシドを、より害の少ない物質へ変換する酵素です。いわば体内に備わった“防錆剤”です。
SODには、細胞質で働くSOD1、ミトコンドリアで働くSOD2など複数のタイプがあります。特にミトコンドリアはエネルギー産生工場である一方、活性酸素も多く発生する場所であり、SOD2の役割は極めて重要です。
この遺伝子が欠損したマウスでは、筋力低下、神経障害、臓器機能低下、フレイル様症状などが早期に現れます。つまり、酸化ストレスを抑えられない体は、年齢以上のスピードで衰えていくのです。
現代の抗老化医学で、運動、睡眠、地中海食、ポリフェノール摂取などが推奨される背景には、この酸化ストレス対策があります。SODは、その中心概念を象徴する遺伝子です。
参考記事:地中海式食事はなぜ“長寿のゴールドスタンダード”なのか──抗老化を加速する食の科学
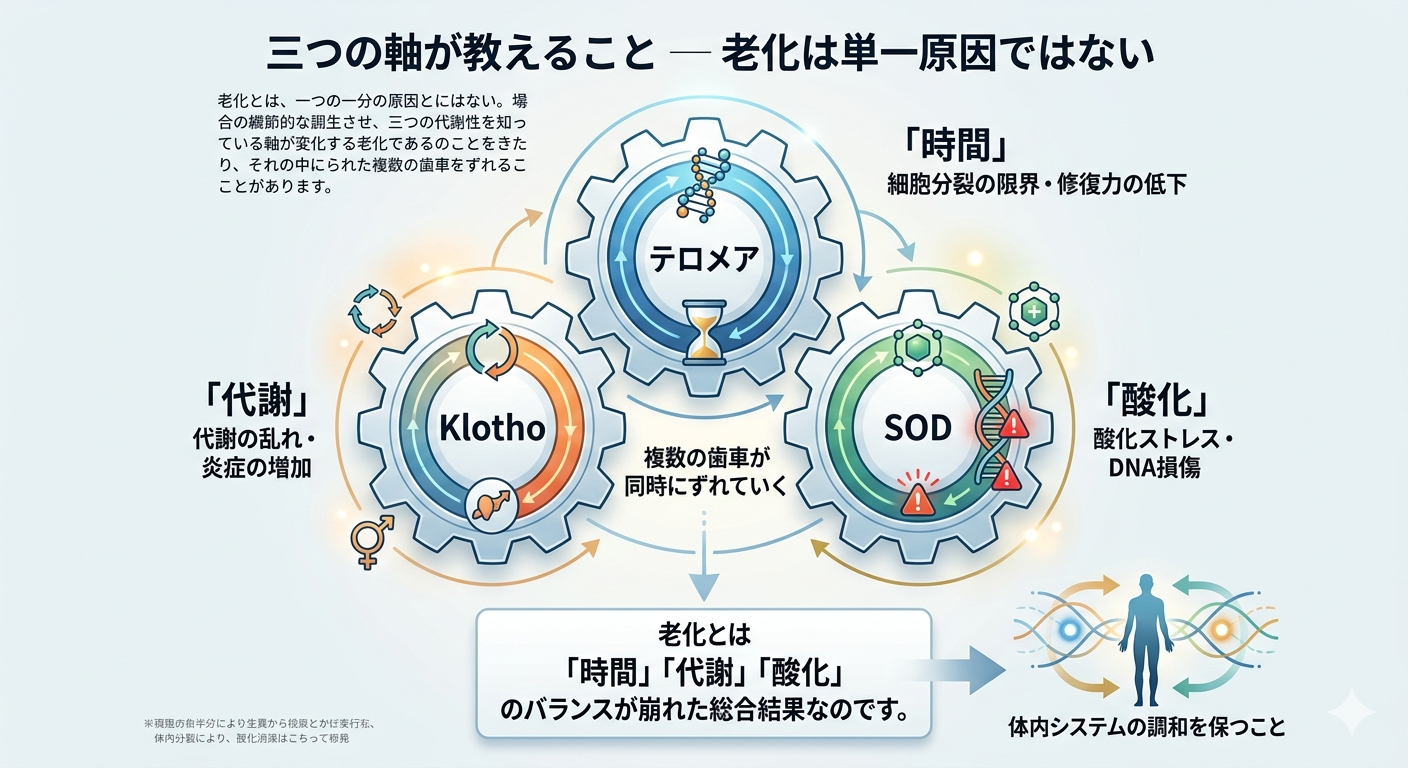
三つの軸が教えること─ 老化は単一原因ではない
テロメアは「時間」、Klothoは「代謝」、SODは「酸化」を象徴しています。これらは別々の話に見えて、実際には密接につながっています。
細胞分裂の限界が近づけば修復力は落ち、代謝が乱れれば炎症が増え、酸化ストレスが高まればDNA損傷が蓄積します。こうして老化は、複数の歯車が同時にずれていくことで進行します。
つまり、老化とは一つの原因で起こる現象ではなく、「時間」「代謝」「酸化」のバランスが崩れた総合結果なのです。
この理解こそが、現代のロンジェビティ戦略の出発点です。若さを保つとは、年齢を止めることではなく、体内システムの調和を保つことに他なりません。
老化遺伝子研究の現在地
─ 見えてきた“老化のネットワーク”
かつて老化は、「年を取れば自然に衰えるもの」と一括りに考えられていました。
ところが現在の研究では、老化は一つの原因で起こる単純な現象ではなく、数百から数千の遺伝子、代謝経路、免疫反応が連動して進む“ネットワーク現象”であることがわかってきました。
たとえるなら、老化は家の中の電球が一つ切れるような故障ではありません。配線、配管、電源、通信システムが少しずつ不調になり、全体として住みにくくなっていく状態に近いものです。現代の抗老化医学は、その複雑な配線図を読み解く段階に入っています。
Sirtuin(サーチュイン)
─ 細胞修復と若さを支える“長寿メンテナンスチーム”
長寿遺伝子として最も有名なのが、Sirtuin(SIRT1〜SIRT7)です。酵母、線虫、マウス、ヒトに至るまで広く存在し、進化的にも保存された重要な仕組みと考えられています。
サーチュインは、DNA修復、炎症抑制、糖代謝、脂質代謝、ミトコンドリア機能の維持など、多方面に関与しています。つまり、一つの仕事だけをする遺伝子ではなく、細胞全体の保守管理を担う“総合メンテナンス部門”です。
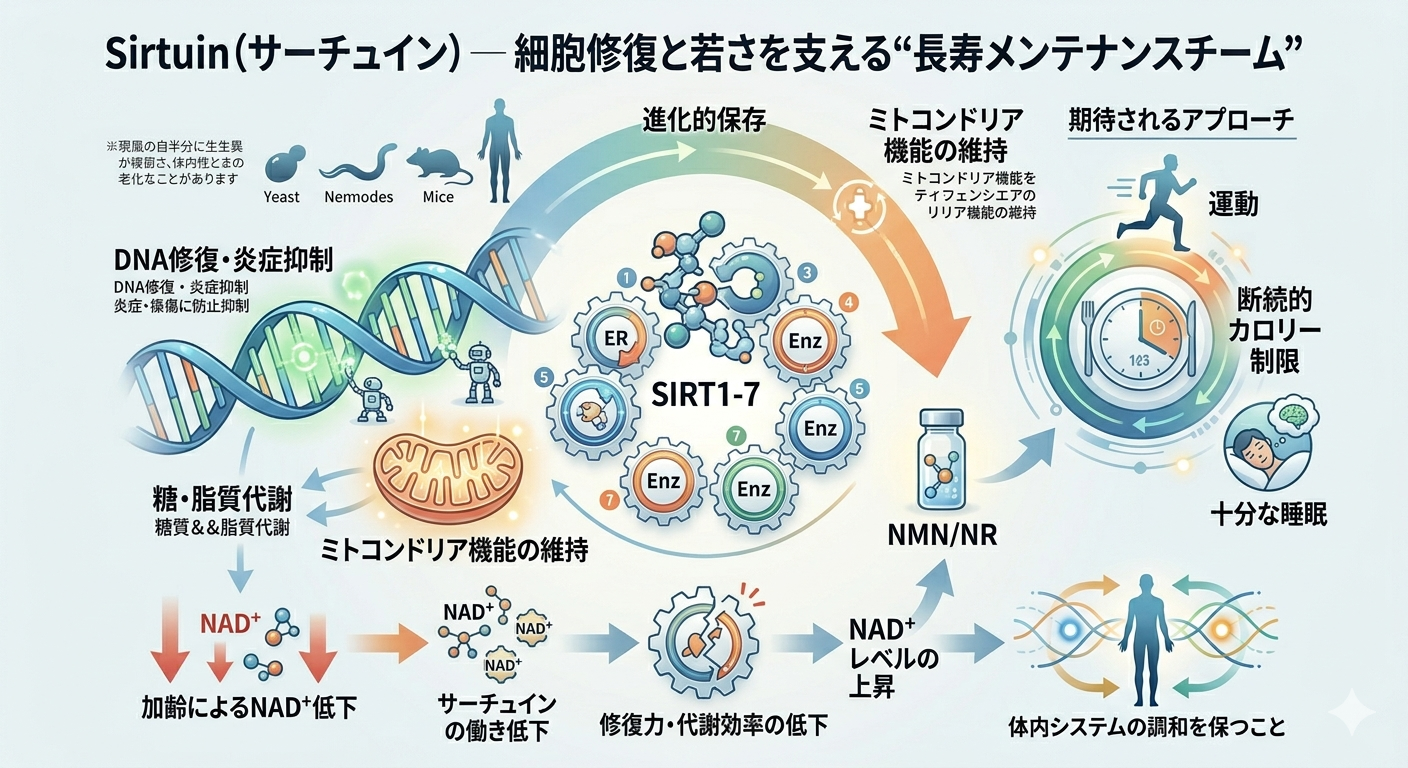
特に注目されるのが、加齢とともに減少しやすいNAD⁺という補酵素との関係です。NAD⁺が低下すると、サーチュインの働きも弱まり、修復力や代謝効率が落ちやすくなると考えられています。
近年は、運動、断続的なカロリー制限、十分な睡眠、NMNやNRなどの研究が進んでいる背景にも、このNAD⁺─サーチュイン経路への期待があります。
BMAL1(時計遺伝子)
─ 生活リズムが老化速度を左右する“体内時計の司令塔”
私たちの身体には、約24時間周期で働く体内時計があります。その中心遺伝子の一つがBMAL1です。
BMAL1は、睡眠と覚醒、体温、ホルモン分泌、血糖調整、細胞修復のタイミングまで幅広く管理しています。いわば、身体の全スタッフに「今は働く時間」「今は修復の時間」と指示を出すタイムキーパーです。
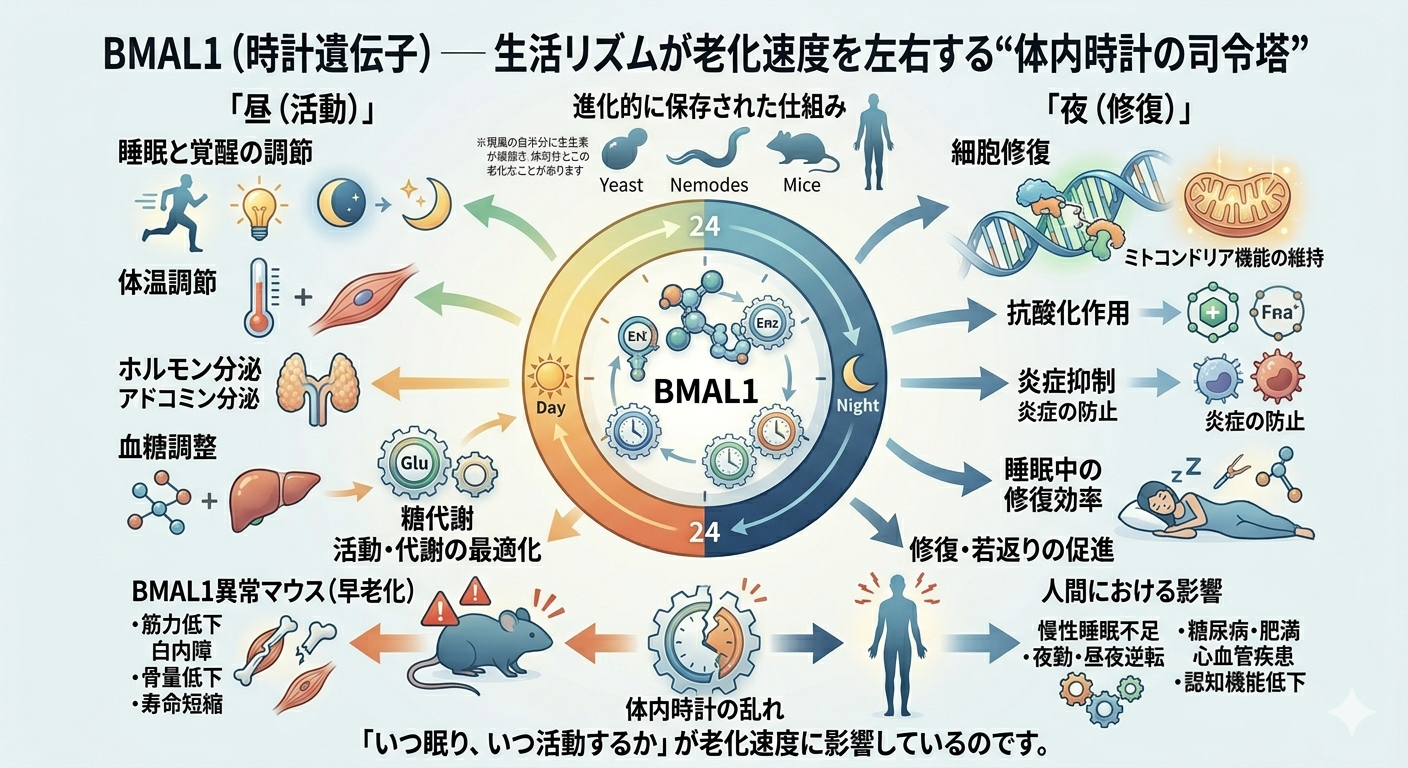
この遺伝子に異常があるマウスでは、筋力低下、白内障、骨量低下、寿命短縮など、早老化に近い変化が確認されています。人間でも、夜勤の継続、慢性的な睡眠不足、昼夜逆転生活が、糖尿病、肥満、心血管疾患、認知機能低下と関連することが知られています。
つまり、何を食べるかと同じくらい、「いつ眠り、いつ活動するか」が老化速度に影響しているのです。
老化細胞関連遺伝子
─ 老化した細胞が周囲まで老けさせる
近年の老化研究で急速に注目されているのが、「老化細胞(Senescent cells)」です。これは傷ついた細胞が増殖を停止しつつ、体内に居座り続ける状態を指します。
本来、細胞老化はがん化を防ぐ安全装置でもあります。しかし加齢とともに老化細胞が蓄積すると、炎症性物質や分解酵素を周囲に放出し、近隣の正常細胞にも悪影響を及ぼします。これをSASP(老化関連分泌現象)と呼びます。
例えるなら、マンションの一室で常に煙や騒音を出し続ける住人がいるようなものです。周囲の住環境まで悪化してしまいます。
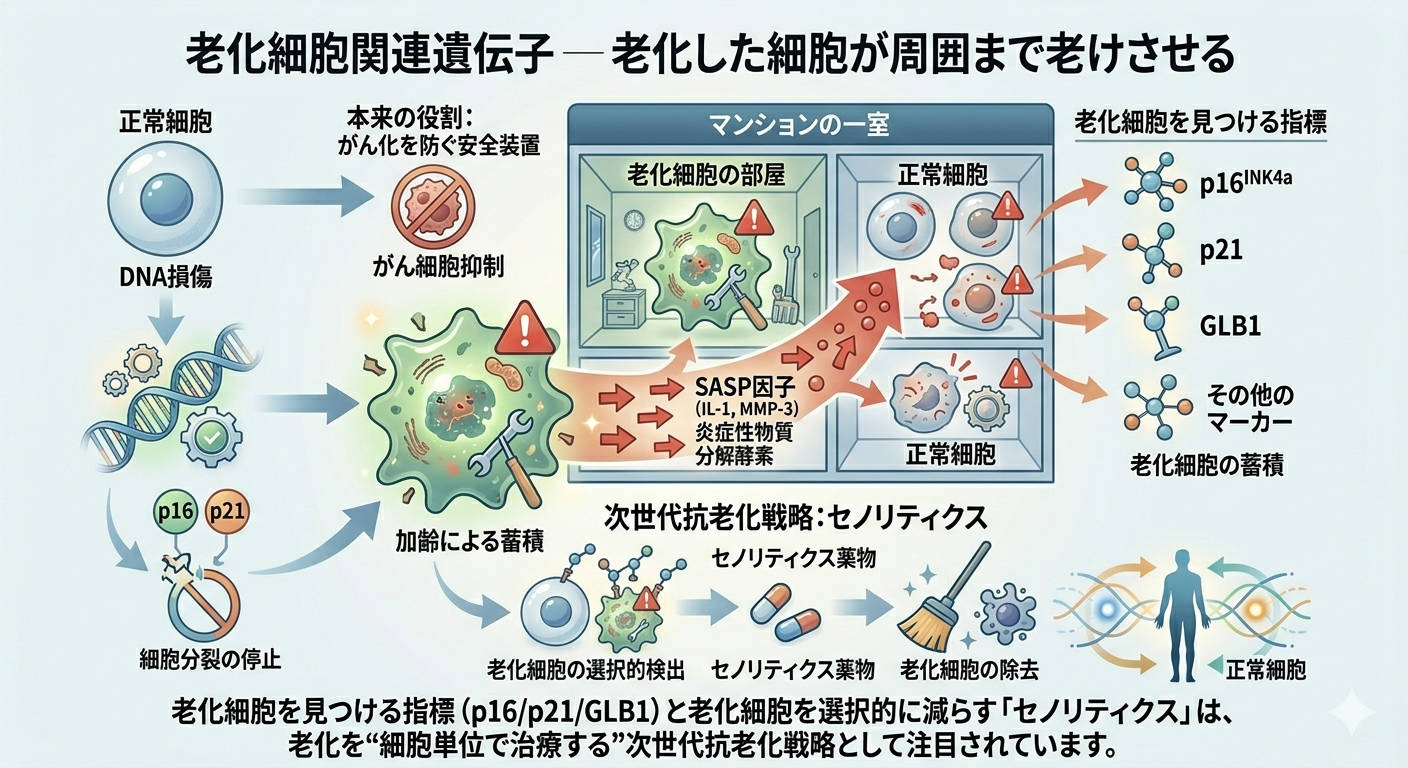
こうした老化細胞を見つける指標として、p16INK4a、p21、GLB1など複数の遺伝子マーカーが研究されています。そして老化細胞を選択的に減らす「セノリティクス」も次世代抗老化戦略として注目されています。
まだ臨床応用は発展途上ですが、老化を“細胞単位で治療する”時代が始まりつつあります。
参考記事:SASP(サスプ)とは何か?セノリティクス時代に知るべき“老化の正体”
参考記事:セノリティクスとは何か?老化細胞(ゾンビ細胞)を除去する最前線と抗老化の未来
炎症・代謝・免疫をつなぐネットワーク
現在の研究で明らかになってきたのは、老化遺伝子は単独で働かないという事実です。
DNA修復が落ちると炎症が増えます。炎症が続くとミトコンドリア機能が低下します。ミトコンドリアが弱るとエネルギー不足になり、さらに修復能力が落ちます。睡眠リズムが乱れれば、この悪循環は加速します。
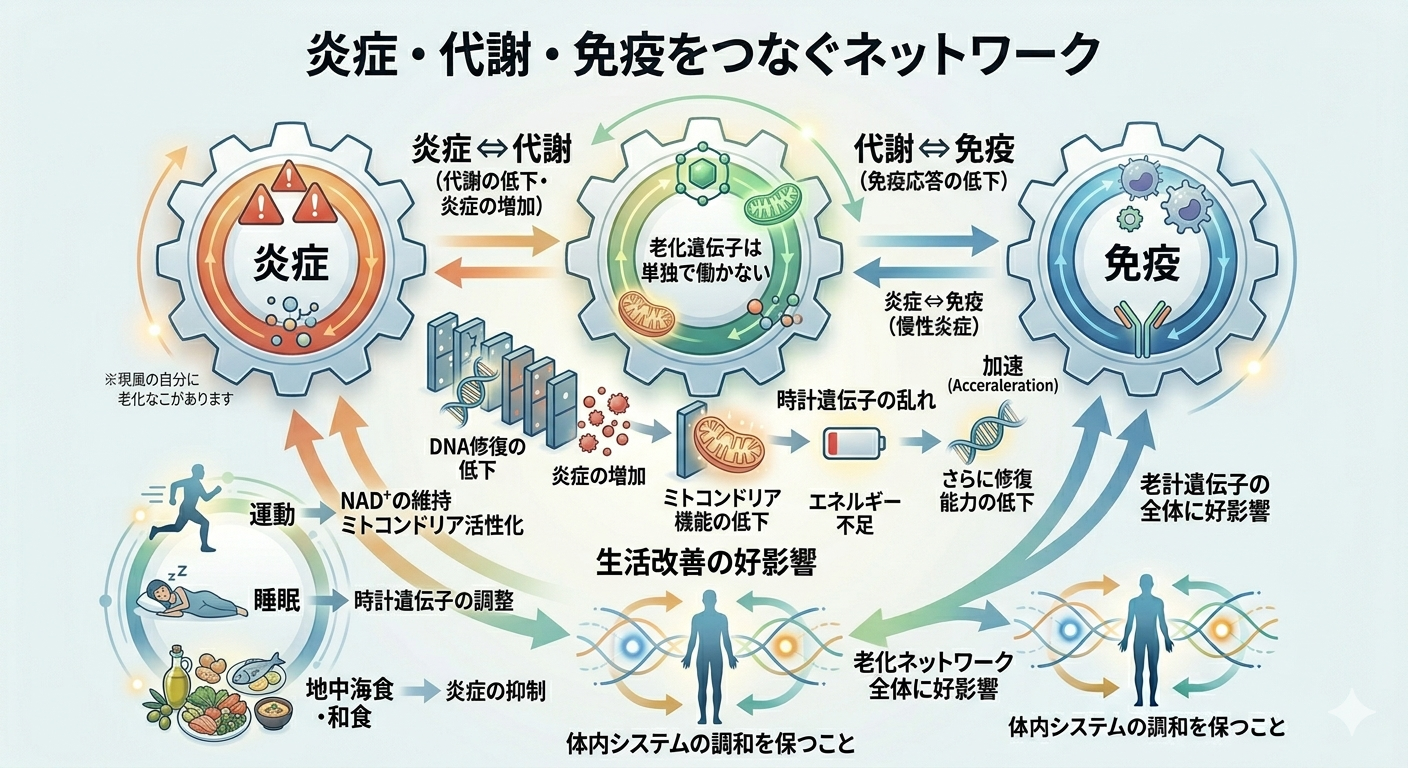
つまり老化とは、ドミノ倒しのように一つの乱れが次の乱れを呼ぶ連鎖反応なのです。逆に言えば、一つの生活改善が複数の経路に良い影響を与える可能性もあります。
運動でNAD⁺が保たれ、睡眠で時計遺伝子が整い、地中海食や和食で炎症が抑えられれば、老化ネットワーク全体に好影響が及ぶという考え方です。
私たちは“老化を読む時代”に入った
以前は、老化は止められないものと考えられていました。今は違います。老化は少しずつ、その構造とルールが見え始めています。
もちろん、すぐに不老不死が実現するわけではありません。しかし、老化を構成するネットワークが理解されれば、健康寿命を延ばし、病気を遠ざけ、活力ある年齢の重ね方を選べる時代に近づきます。
老化遺伝子研究の現在地とは、「人はなぜ老いるのか」という問いに対し、初めて具体的な地図が描かれ始めた地点なのです。

未来展望─ 老化は「治療する時代」へ
老化遺伝子研究は、今まさに臨床応用の入り口に立っています。
長寿遺伝子を活性化する栄養・生活習慣の最適化、老化細胞の選択的除去、さらには遺伝子発現そのものを制御する治療。
これらはすでに研究段階から実装段階へと移行しつつあります。
重要なのは、老化が「不可逆な現象」ではなく、「介入可能なプロセス」に変わりつつあるという点です。
かつて感染症が克服され、がんが制御されつつあるように、次に人類が向き合うのは「老化そのもの」なのかもしれません。
まとめ
老化は“運命”ではなく“設計可能”な時代へ
老化遺伝子の研究は、私たちに重要な視点をもたらしました。
それは、老化とは単なる時間の経過ではなく、「修復」「維持」「調整」というシステムのバランスの結果であるということです。
そしてそのバランスは、完全ではないにせよ、食事・運動・生活習慣によってある程度コントロール可能であることもわかってきました。
未来の医療は、「病気を治す」だけではなく、「老化を遅らせる」「若さを維持する」という方向へ確実に進んでいます。
私たちは今、老化の仕組みを“知る側”から“扱う側”へと移行する過渡期にいます。
ロンジェビティとは、特別な才能ではなく、科学を理解し、日常に落とし込む力そのものです。
その第一歩は、「老化はコントロールできるかもしれない」と知ることから始まります。
参考文献:アンチエイジング医学の基礎と臨床 第4版「老化遺伝子とアンチエイジング」

