ミトコンドリアが寿命を左右する?抗老化のカギを握る細胞エネルギーの正体

「年齢とともに疲れやすくなる」「回復力が落ちる」
こうした変化は、単なる体力の問題ではなく、細胞レベルの変化によって引き起こされています。
その中心にあるのが「ミトコンドリア」です。
ミトコンドリアはエネルギー産生の場として知られていますが、近年ではそれにとどまらず、老化・寿命・疾患の発症にまで関与する“生体の制御装置”として注目されています。
さらに、サーチュイン(長寿遺伝子)やAMPK、mTORといった栄養応答シグナルとの連携により、ミトコンドリアは老化の進行速度を左右する重要なハブとなっています。
本稿では、ミトコンドリアの基礎から、分子レベルの制御機構、さらには薬剤介入までを体系的に整理し、抗老化医学の中核としての役割を解説します。
ミトコンドリアとは何か?(エネルギー代謝の本質)
ミトコンドリアは、細胞内に存在するエネルギー産生装置であり、生命活動の根幹を支えています。
- TCA回路(クエン酸回路)
糖質や脂質、アミノ酸から生成された代謝産物を酸化し、電子伝達系へとつなぐ中心的経路です。ここで生じる還元当量(NADHやFADH₂)が、後続のATP産生の原動力となります。 - 脂肪酸β酸化
脂肪酸を分解し、アセチルCoAへと変換するプロセスです。特に空腹時や運動時にはこの経路が活性化し、持続的なエネルギー供給を担います。 - 酸化的リン酸化(OXPHOS)
電子伝達系を通じてプロトン勾配を形成し、ATPを産生する最終段階です。ここが破綻するとエネルギー不足だけでなく、活性酸素の過剰産生にもつながります。
これらの経路は独立しているわけではなく、相互に密接に連携しながら、細胞のエネルギー需要に応じて柔軟に調整されています。
ミトコンドリアは“老化のハブ”である
ミトコンドリアは単なる代謝器官ではなく、老化の進行に関わる複数の重要機能を担っています。
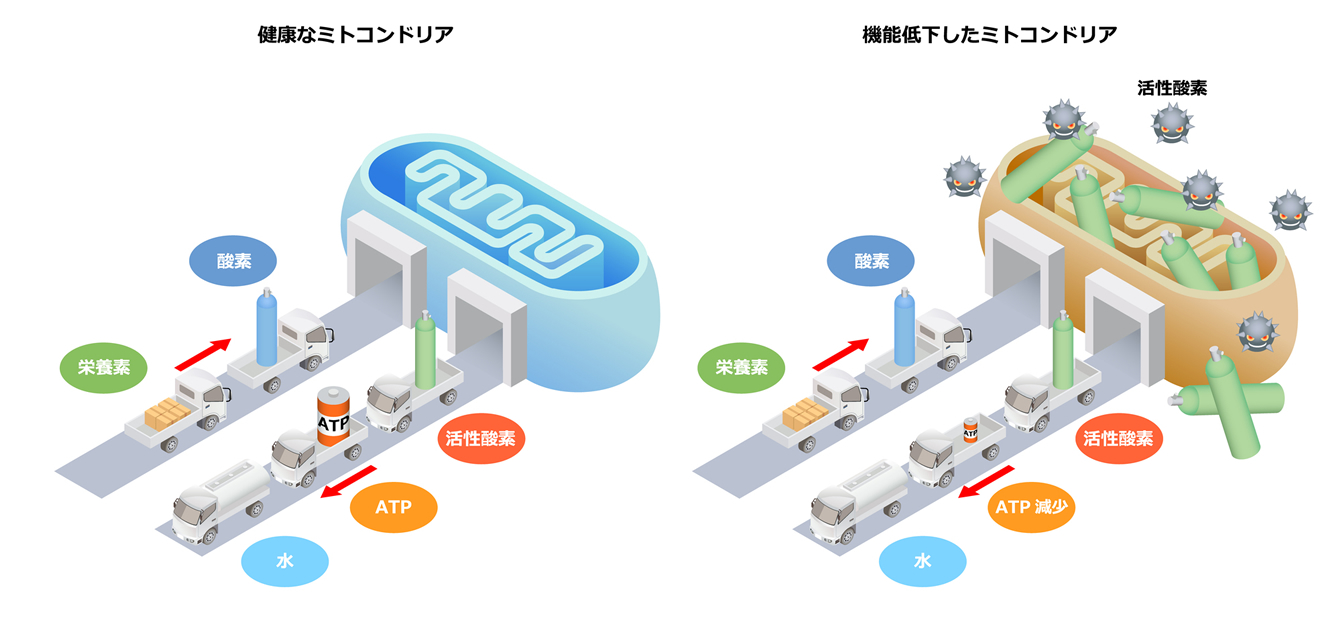
- 活性酸素(ROS)の産生と制御
ミトコンドリアはATP産生の過程でROSを生じます。適量のROSはシグナル伝達に必要ですが、過剰になるとDNAやタンパク質を損傷し、老化を促進します。 - ミトコンドリアDNA(mtDNA)の維持
ミトコンドリア独自のDNAは核DNAよりも損傷を受けやすく、修復機構も限定的です。そのため、加齢に伴い変異が蓄積しやすい特徴があります。 - マイトファジー(品質管理)
損傷したミトコンドリアを選択的に分解・除去する仕組みです。この機能が低下すると、不良ミトコンドリアが蓄積し、細胞機能全体の低下につながります。 - テロメアおよび細胞老化との連動
ミトコンドリア機能低下はテロメア短縮や細胞老化シグナルを誘導し、全身の老化プロセスに波及します。
このように、ミトコンドリアは複数の老化メカニズムの“交差点”として機能しています。
ミトコンドリア機能の低下=老化の進行
加齢に伴うミトコンドリア機能の低下は、さまざまな慢性疾患の共通基盤となります。
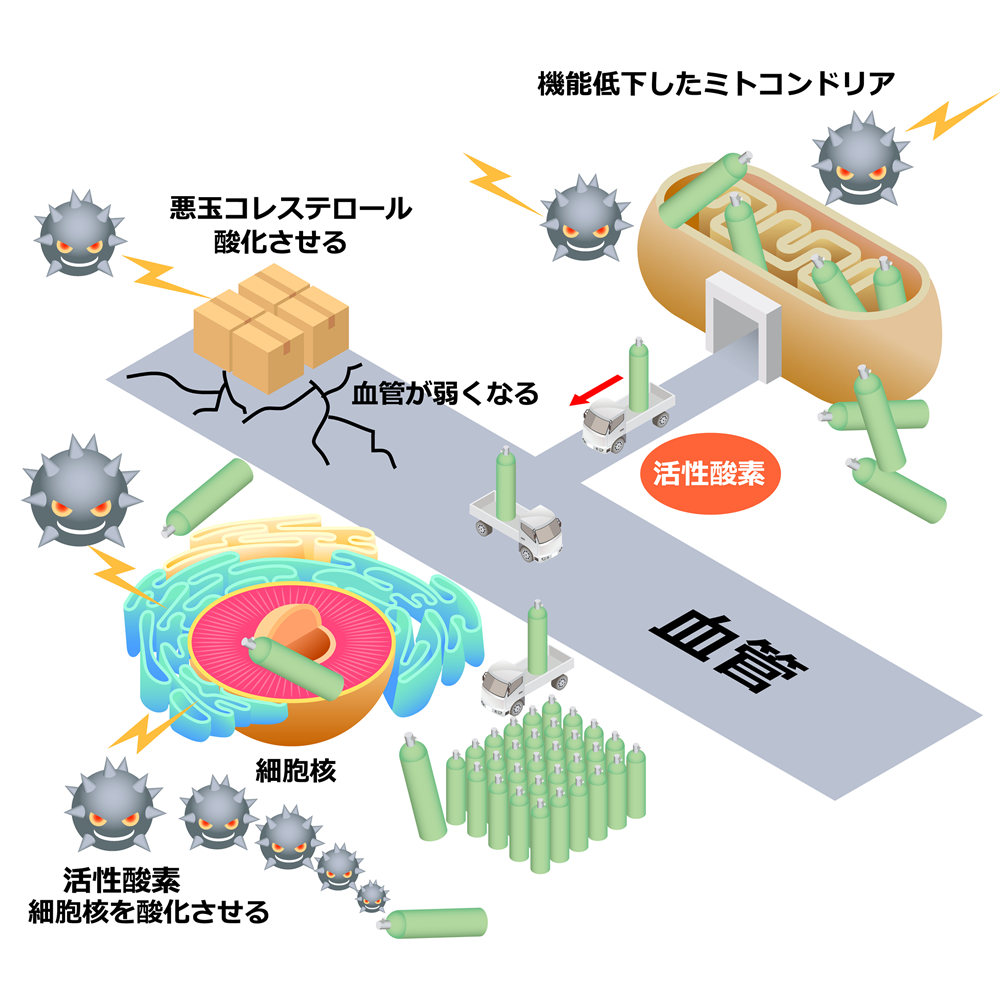
- 糖尿病
インスリン抵抗性の背景には、ミトコンドリアでの脂肪酸代謝異常が関与しています。エネルギー利用効率の低下が代謝全体の乱れを引き起こします。 - 心不全
心筋は大量のエネルギーを必要とするため、ミトコンドリア機能低下は直接的に収縮力の低下へとつながります。 - 神経変性疾患(アルツハイマー病など)
神経細胞はエネルギー依存性が高く、ミトコンドリア障害はシナプス機能低下や細胞死を誘導します。
これらの疾患に共通するのは、「エネルギー代謝の破綻」と「慢性炎症」です。ミトコンドリアはその両方に関与しています。
寿命を決める「シグナル」とミトコンドリア
老化や寿命を制御する分子ネットワークは、ミトコンドリア機能と密接に連動しています。
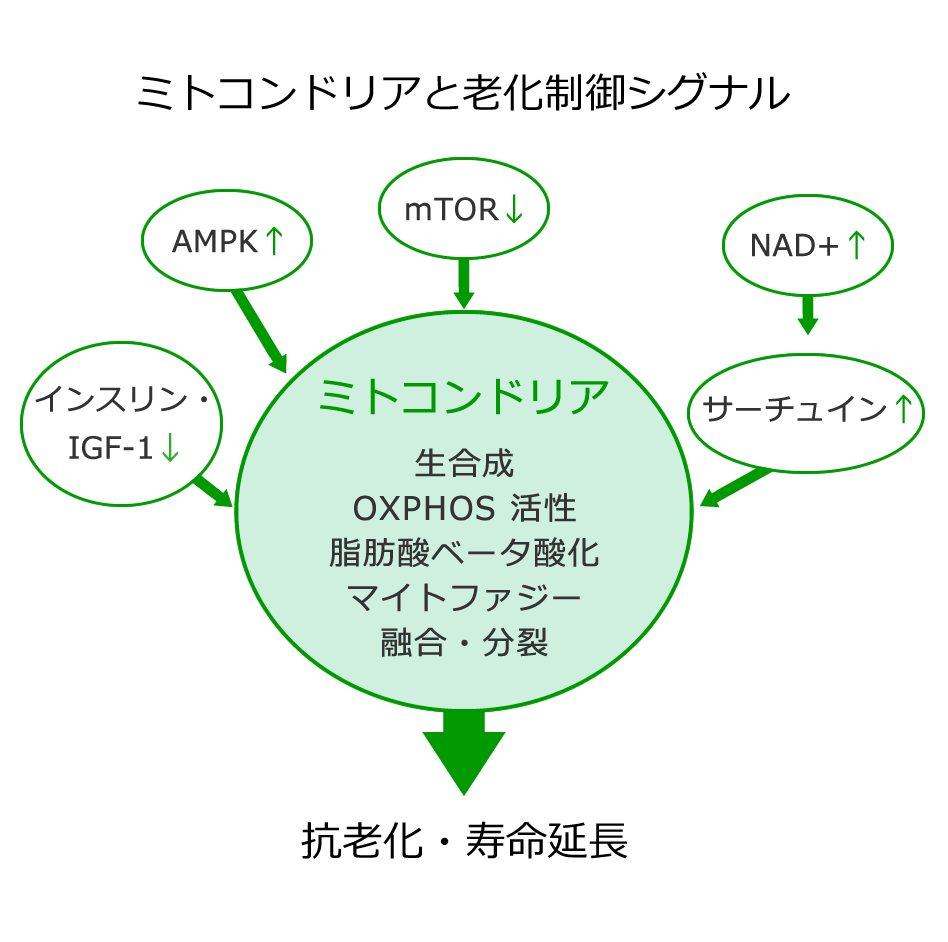
- AMPK(エネルギーセンサー)
細胞内のエネルギー不足(AMP/ATP比上昇)で活性化し、エネルギー産生を促進する方向に働きます。PGC-1αを介してミトコンドリア新生を促進し、「省エネかつ効率的な代謝」へとシフトさせます。 - IGF-1シグナル
栄養豊富な状態で活性化しますが、その抑制はFOXO転写因子を活性化し、ストレス耐性やミトコンドリア機能を向上させる方向に働きます。 - mTOR(栄養センサー)
細胞成長と合成を促進する一方で、過剰活性化は老化促進と関連します。特にオートファジー抑制を通じて、ミトコンドリアの質の低下を招きます。
これらは単独ではなく、相互に影響し合うネットワークとして機能しています。
メトホルミンとmTOR阻害薬(ラパマイシン)
こうしたシグナルに介入する薬剤として注目されているのが、
- メトホルミン
AMPKを活性化し、ミトコンドリア代謝を改善します。糖代謝の改善に加え、慢性炎症の抑制や寿命延長効果が報告されています。 - ラパマイシン(mTOR阻害薬)
mTORC1を抑制し、オートファジーを促進します。これによりミトコンドリアの品質管理が改善され、老化の進行を遅らせる可能性があります。
これらの薬剤は、ミトコンドリア機能を“間接的に最適化する”戦略として注目されています。
サーチュインとミトコンドリアのクロストーク
サーチュインは、ミトコンドリア機能と老化制御をつなぐ中核的存在です。
- SIRT1(核・細胞質)
PGC-1αを活性化し、ミトコンドリア新生を促進します。またFOXOやAMPKとも連携し、全身の代謝バランスを調整します。 - SIRT3〜5(ミトコンドリア内)
エネルギー代謝酵素の活性を直接制御し、ROS産生を抑制します。特にSIRT3は抗酸化作用において重要です。 - SIRT6・SIRT7など
DNA修復や炎症制御を通じて、間接的にミトコンドリア機能を支えます。
これらは単独で働くのではなく、AMPKやmTORとクロストークを形成しながら機能しています。
NAD+と抗老化戦略
サーチュイン活性の鍵を握るのがNAD+です。

- NAD+の役割
エネルギー代謝だけでなく、サーチュインの活性化に必須の補酵素です。 - 加齢による低下
NAD+は加齢とともに減少し、ミトコンドリア機能低下の一因となります。 - 補充戦略(NMNなど)
NAD+前駆体の補充により、サーチュイン活性を回復させ、ミトコンドリア機能を改善する可能性が示唆されています。
まとめ
ミトコンドリアは、単なるエネルギー工場ではなく、老化・寿命・疾患のすべてに関わる「生命の制御装置」です。

その機能は、サーチュイン、AMPK、mTORといった分子ネットワークによって精密に調整され、さらに薬剤や生活習慣によって介入可能であることがわかってきました。
つまり私たちは今、老化を“結果”として受け入れる時代から、“制御する対象”として扱う時代へと移行しつつあります。
そしてその中心にあるのが、ミトコンドリアです。
日々の生活習慣から最先端医療まで、あらゆるアプローチがミトコンドリアに収束していく時代。
この視点を持つことが、これからの抗老化戦略を考えるうえで、確かな羅針盤になるはずです。
この記事を書いた人
1978年生まれ、京都府出身。看護師として京都市内の病院に8年間勤務後、上京。東京都内の総合病院にてICU(集中治療室)、NICU(新生児集中治療室)、手術室での高度急性期医療に従事。看護師プリセプターとして後進の育成にも尽力する。
臨床現場での経験から、既存の制度では対応困難なニーズを痛感し、24時間対応保育所や自費訪問看護ステーションを自ら立ち上げた起業家としての側面も持つ。
現在は、訪問看護の発展を支援する総合Webメディア「いろいろナース」および、抗老化とロンジェビティ(長寿科学)の実践をガイドする「こもれび抗老化ステーション」の編集長を務める。医療現場のリアルな知見と最新のロンジェビティ理論を融合させ、日本人の健康寿命延伸に寄与する情報発信を行っている。


“ミトコンドリアが寿命を左右する?抗老化のカギを握る細胞エネルギーの正体” に対して2件のコメントがあります。
コメントは受け付けていません。