エピジェネティッククロックとは何か?生物学的年齢を測る最新科学を徹底解説

同じ年齢なのに、なぜ人によって「若さ」に差があるのでしょうか。
見た目や体力だけでなく、病気のなりやすさや回復力にも明確な違いが存在します。
この“差”の正体こそが、「生物学的年齢」です。
そして現在、この生物学的年齢を最も精度高く測定できるとされているのが
エピジェネティッククロックという技術です。
老化は単なる時間の経過ではありません。
それは、私たちの細胞の中で静かに進む“情報の変化”です。
本コラムでは、この「エピジェネティッククロック」という概念がどのように生まれ、どのような仕組みで老化を測定し、そして未来の医療をどう変えていくのかを、初心者にもわかりやすく、かつ専門的な視点から深く解説していきます。
老化の本質は「遺伝子の使い方の変化」である
私たちは通常、老化を「時間の経過」として捉えています。
しかし、生物学的にはそれだけでは説明がつきません。
同じ年齢でも健康状態が大きく異なるのは、細胞レベルで起きている“分子の変化”に違いがあるからです。
その中心にある概念がエピジェネティクスです。
エピジェネティクスとは何か
エピジェネティクスとは、DNAの配列そのものを変えることなく、遺伝子の働き方を調整する仕組みです。
私たちの体は同じDNAを持っていても、細胞ごとに異なる役割を果たしています。
その違いを生み出しているのが、このエピジェネティクスです。
たとえるなら、DNAが「同じ種」だとすれば、エピジェネティクスは「その種が育つ環境」にあたります。
同じ種でも、光や水、土壌の違いによって成長の仕方が変わるように、遺伝子もまた、置かれた環境によって働き方が変化します。
その代表的な仕組みが「DNAメチル化」です。
DNA上の特定の領域(CpGサイト)にメチル基(CH₃)が付加されることで、遺伝子のスイッチが調整され、発現が抑えられたり、活性化されたりします。
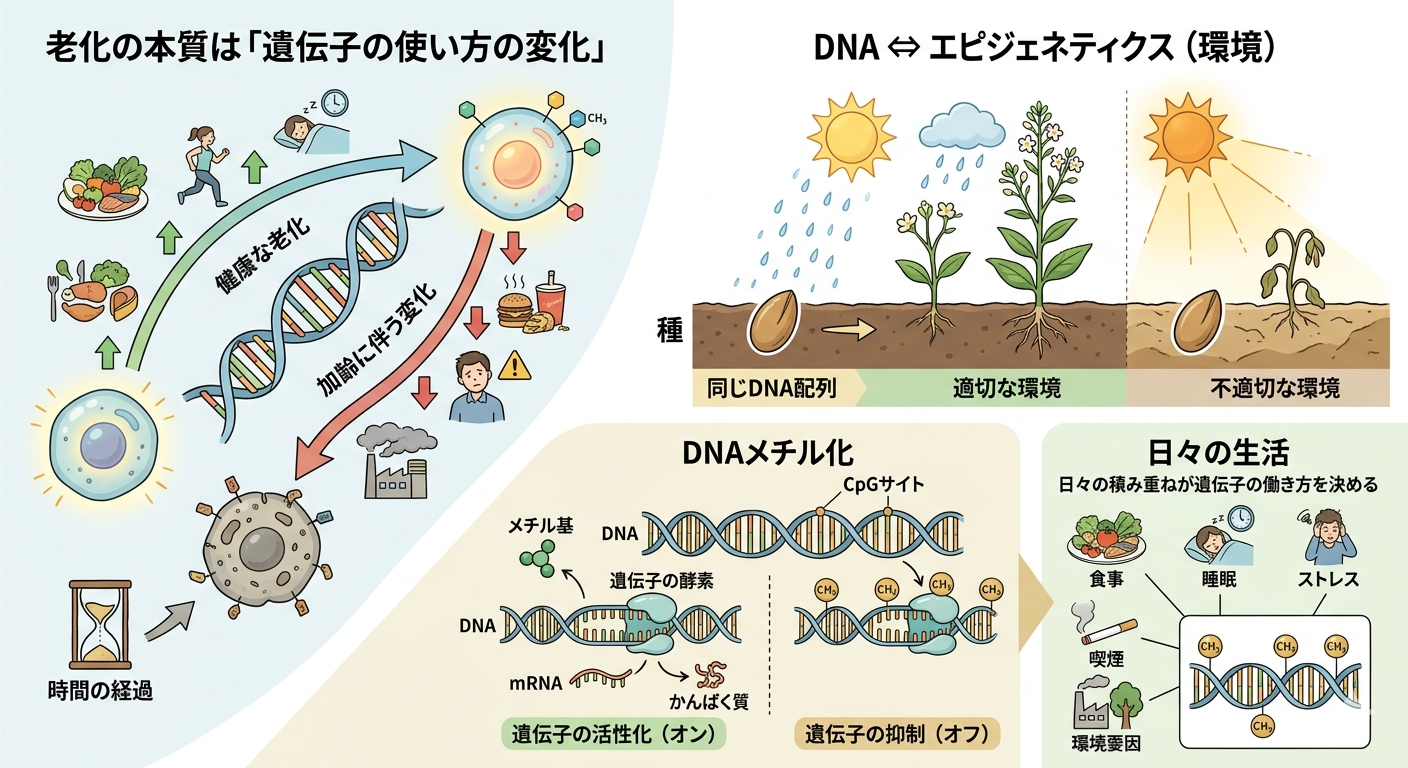
重要なのは、このメチル化の状態が固定されたものではなく、日々の生活によって変化する“動的な情報”であるという点です。
たとえば、食事、睡眠、ストレス、喫煙、環境要因といった日常の積み重ねが、メチル化のパターンに影響を与えます。
つまり私たちの生き方そのものが、遺伝子の働き方に静かに書き込まれているのです。
エピジェネティッククロックとは何か
このDNAメチル化のパターンを解析し、「体の本当の年齢=生物学的年齢」を算出する技術が
エピジェネティッククロック(Epigenetic Clock)です。
AIや機械学習を用いて、特定のCpGサイトのメチル化状態から年齢を推定します。
この技術の重要なポイントは、単なる年齢推定にとどまらないことです。
暦年齢と生物学的年齢のズレ(エイジギャップ)
エピジェネティッククロックによって、次のような“差”が明らかになります。
- 実年齢より若い → 老化が遅い
- 実年齢より高い → 老化が進んでいる
この差は「エイジギャップ」と呼ばれ、健康状態や将来リスクを強く反映します。
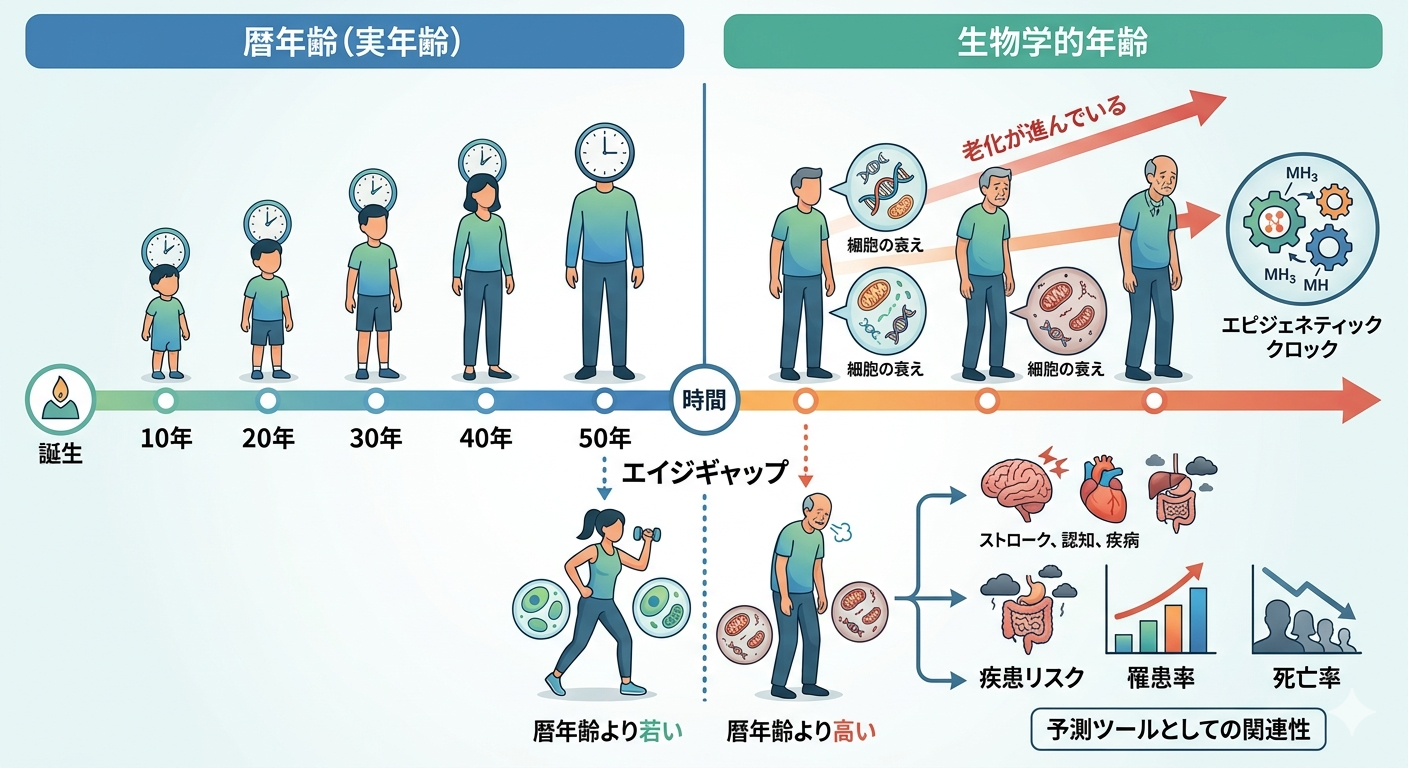
近年の研究では、
- 疾患リスク
- 罹患率
- 死亡率
とも強く関連することが示されており、単なる指標ではなく「予測ツール」として注目されています。
エピジェネティッククロックの誕生と進化
この分野は比較的新しく、急速に進化しています。
- 2011年:DNAメチル化による年齢予測が可能と判明
- 2013年:エピジェネティッククロック概念が提唱
その後、以下のように進化してきました。
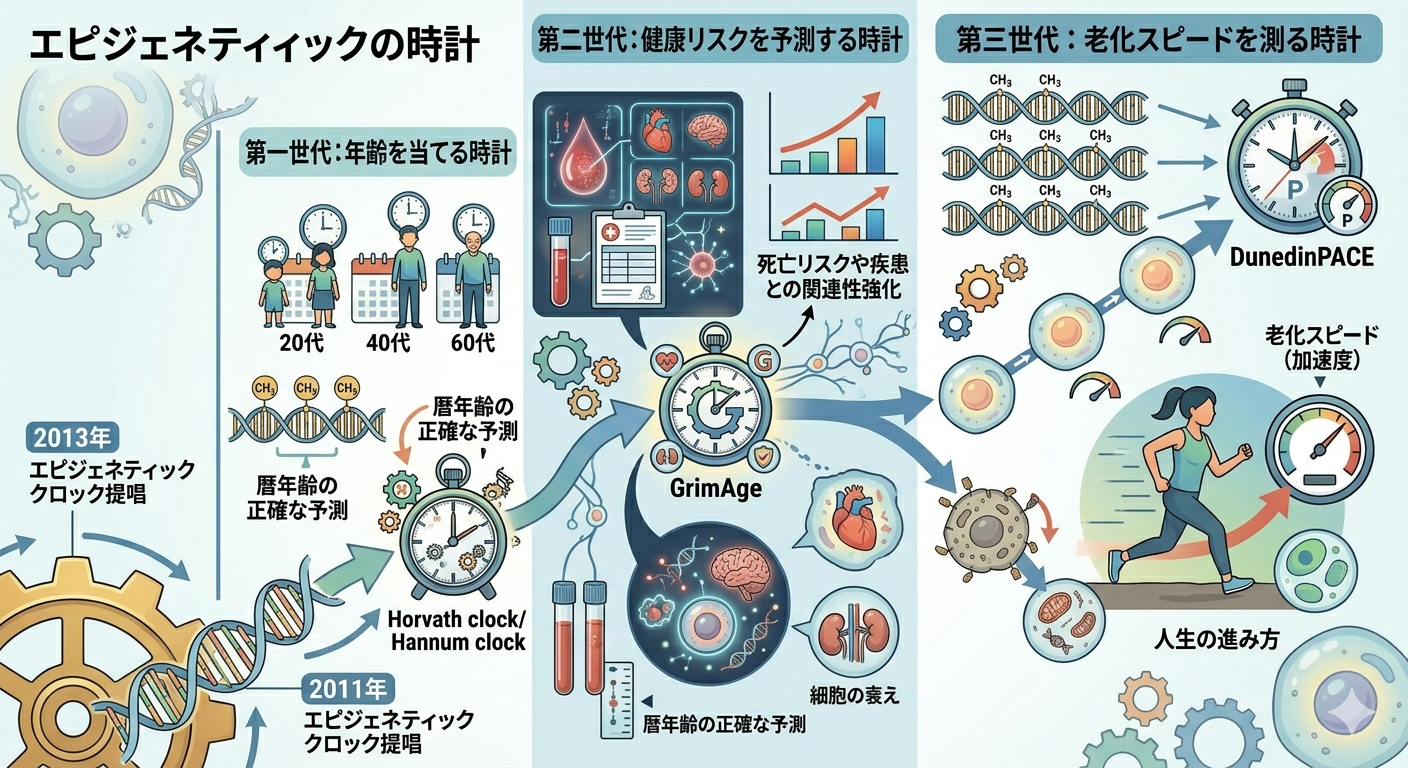
第一世代:年齢を当てる時計
代表例:Horvath clock、Hannum clock
特定のCpG領域のメチル化から「暦年齢をどれだけ正確に予測できるか」に焦点。
第二世代:健康リスクを予測する時計
代表例:GrimAge
血液データなどの臨床情報を組み合わせ、死亡リスクや疾患との関連性を強化。
第三世代:老化スピードを測る時計
代表例:DunedinPACE
「今どれくらい老化しているか」だけでなく、どれくらいの速度で老化しているか(加速度)を測定。
これはまさに、“人生の進み方そのもの”を測る指標と言えます。
DNAメチル化時計の仕組み
──“膨大な遺伝子の中から、老化のサインだけを拾い上げる技術”
エピジェネティッククロックの核心は、「どのDNAの変化を見れば“年齢”がわかるのか」を特定した点にあります。
私たちのDNAには約30億塩基対が存在し、その中には数千万規模のCpGサイト(メチル化が起こる場所)が点在しています。
つまり本来、老化の情報は“膨大すぎてそのままでは扱えない”のです。
では、どのようにして「年齢を示すシグナル」だけを抽出しているのでしょうか。
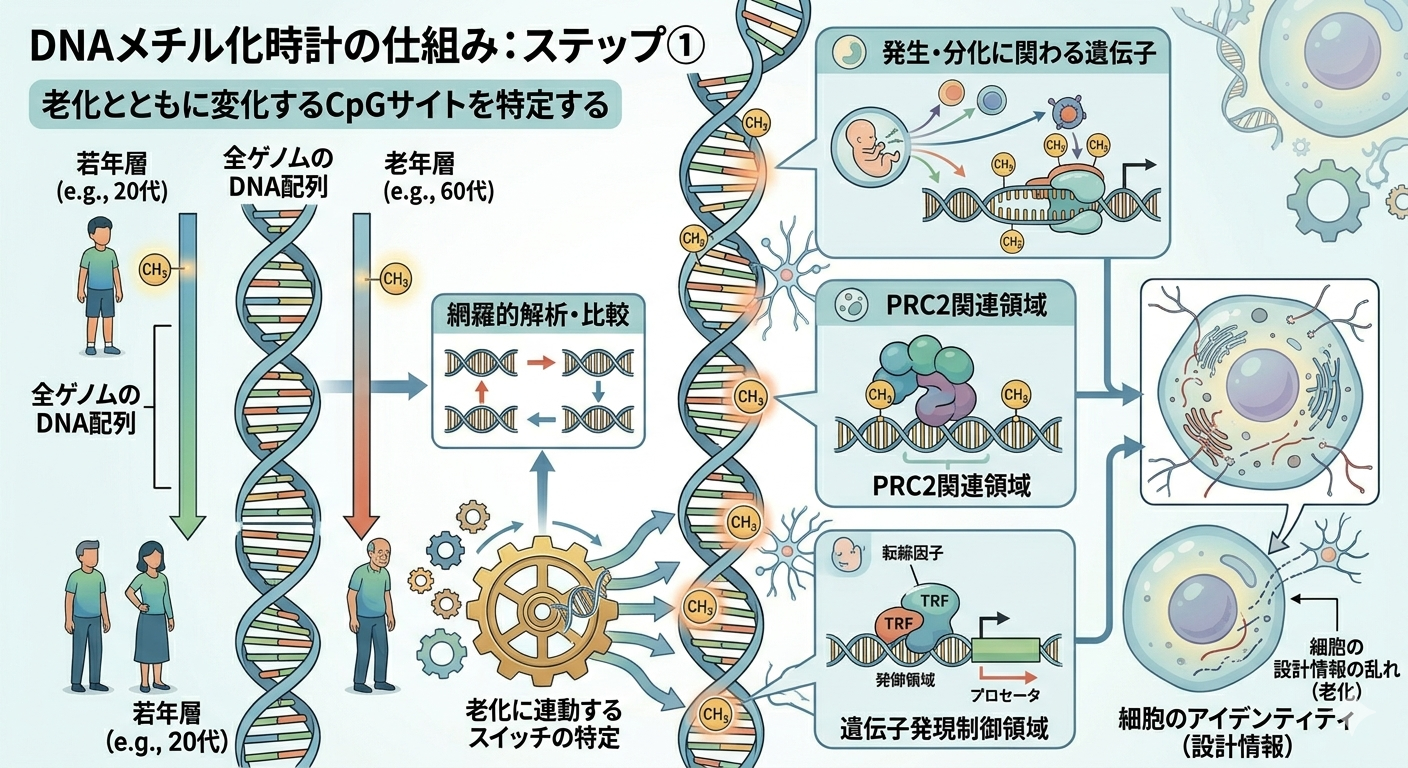
ステップ①:老化とともに変化するCpGサイトを特定する
まず研究者たちは、異なる年齢の人々のDNAを網羅的に解析し、「年齢とともに一貫して変化するCpGサイト」を探し出しました。
これは、いわば“老化に連動して動くスイッチ”を見つける作業です。
興味深いのは、これらのCpGサイトがランダムに選ばれているわけではない点です。
- 発生や分化に関わる遺伝子領域
- ポリコーム抑制複合体(PRC2)関連領域
- 遺伝子発現の制御に重要な領域
といった、“細胞のアイデンティティ”に関わる場所に多く存在しています。
つまりエピジェネティッククロックは、単なる劣化ではなく、細胞の設計情報の乱れを捉えているのです。
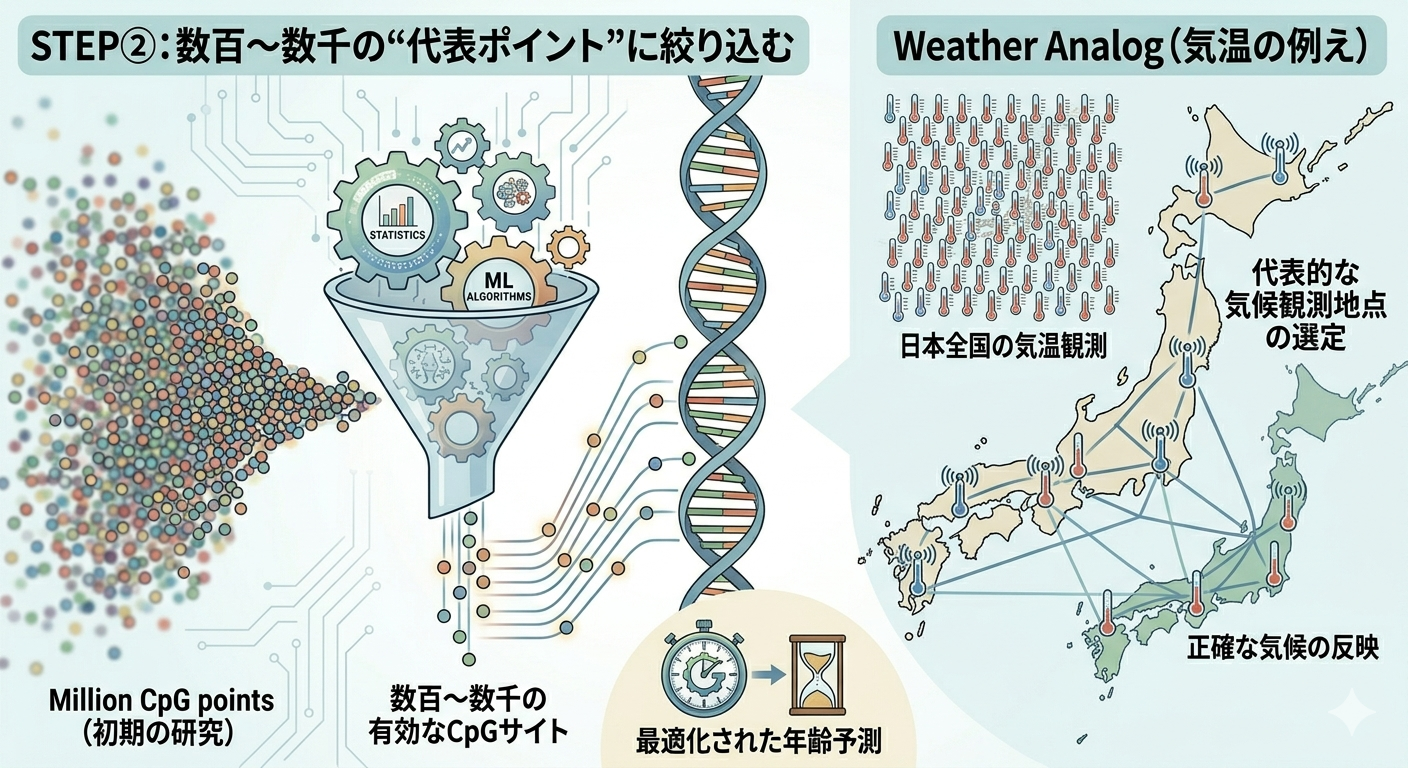
ステップ②:数百〜数千の“代表ポイント”に絞り込む
初期の研究では数百万のCpGサイトが対象でしたが、現在ではその中から年齢予測に最も有効な数百〜数千箇所に絞り込まれています。
例えるなら、「日本全国の気温を全部測る」のではなく、“気候を最も正確に反映する観測地点”だけを選ぶようなものです。
この選定には統計学と機械学習が用いられ、「どの組み合わせが最も正確に年齢を予測できるか」が最適化されています。
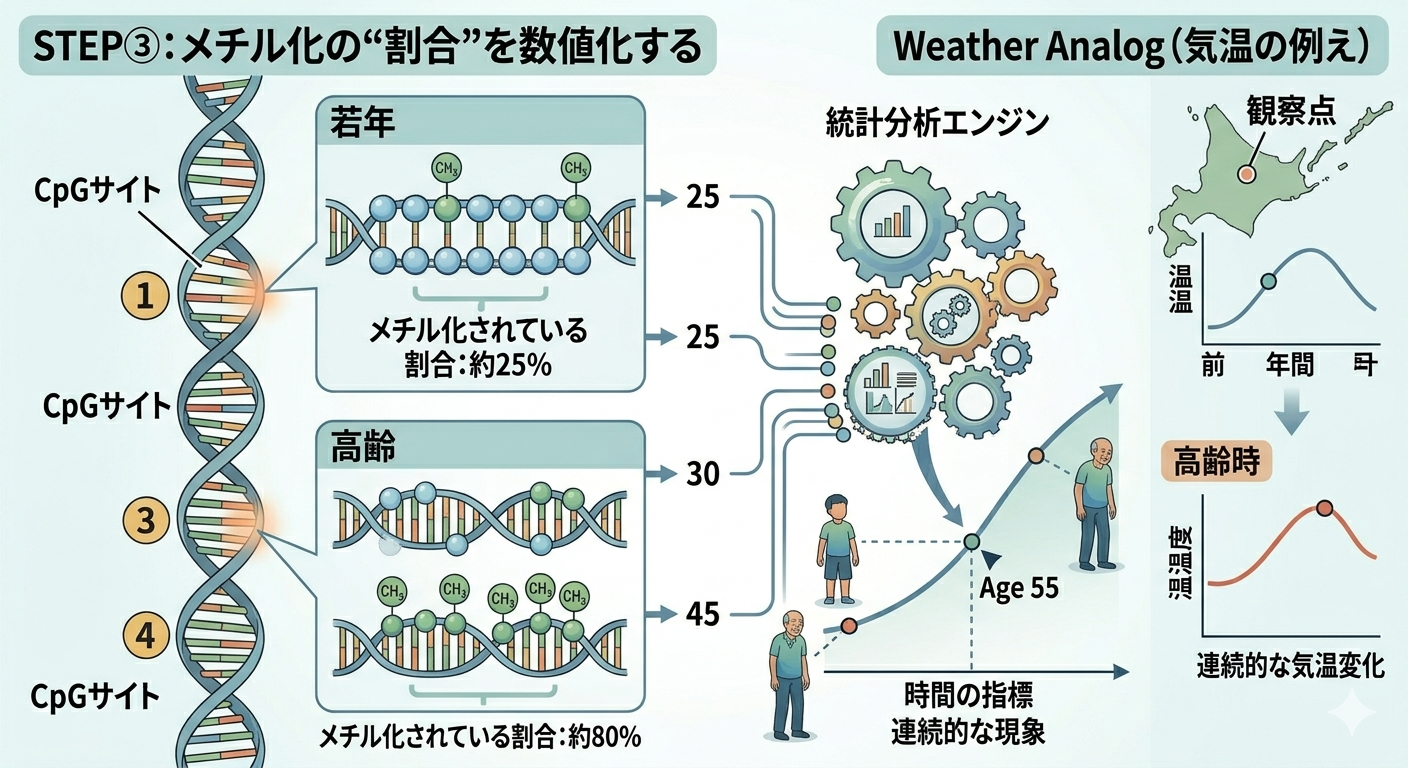
ステップ③:メチル化の“割合”を数値化する
各CpGサイトでは、
- メチル化されている割合(%)
が測定されます。
重要なのは、「オンかオフか」ではなくどの程度メチル化されているか(連続的な値)で評価する点です。
例えばある部位が、
- 若年では10%
- 高齢では70%
と変化する場合、その割合自体が「時間の指標」になります。
このような微細な変化を積み重ねることで、年齢という“連続的な現象”を再現しているのです。
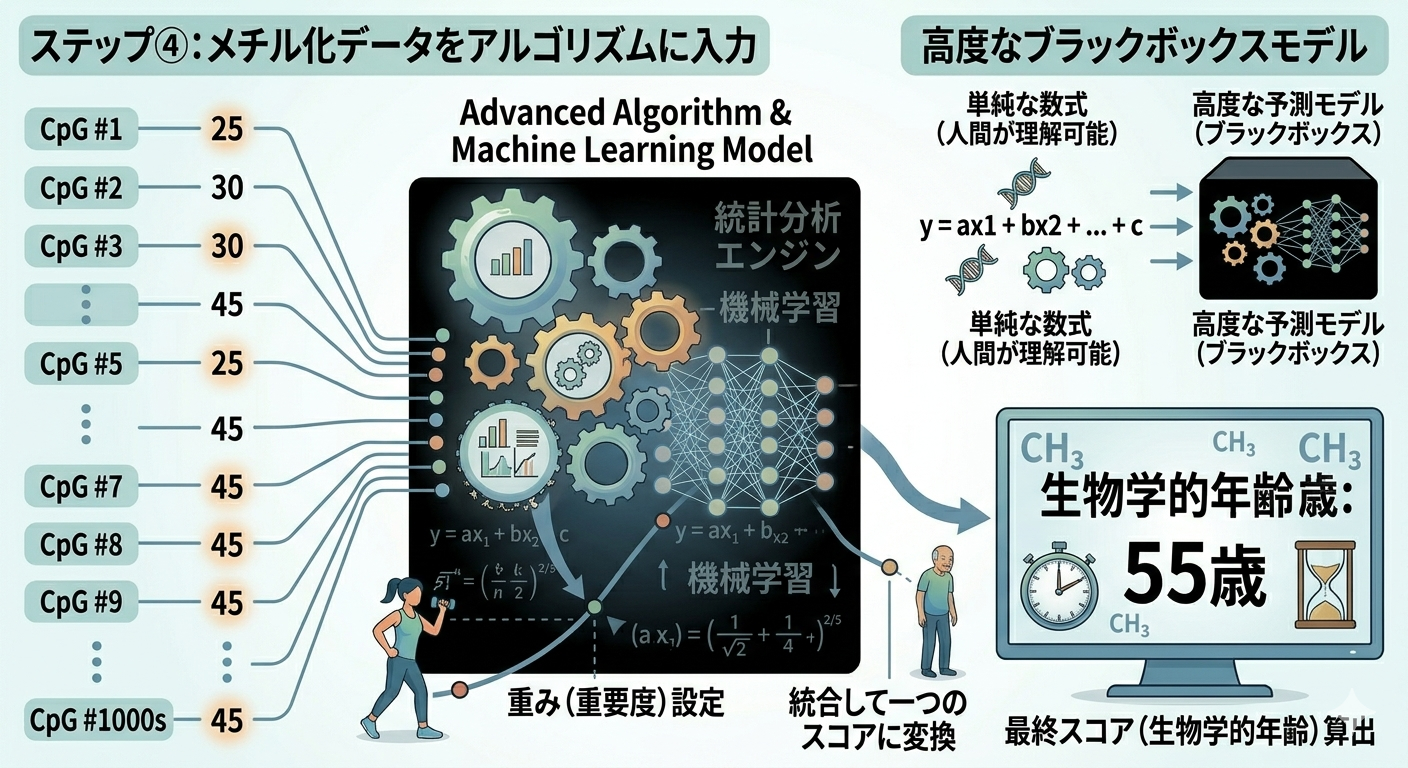
ステップ④:アルゴリズムで年齢に変換する
選ばれたCpGサイトのメチル化データは、エピジェネティッククロックごとに定義された数式(アルゴリズム)に入力されます。
代表的なモデルでは、
- 各CpGサイトに重み(重要度)が設定されており
- それらを統合して一つのスコアに変換
することで、最終的に「生物学的年齢」が算出されます。
ここで使われるのが機械学習です。
膨大なデータから導かれたこの計算式は、人間が直感的に理解できる単純な仕組みではなく、“ブラックボックス”に近い高度な予測モデルとなっています。
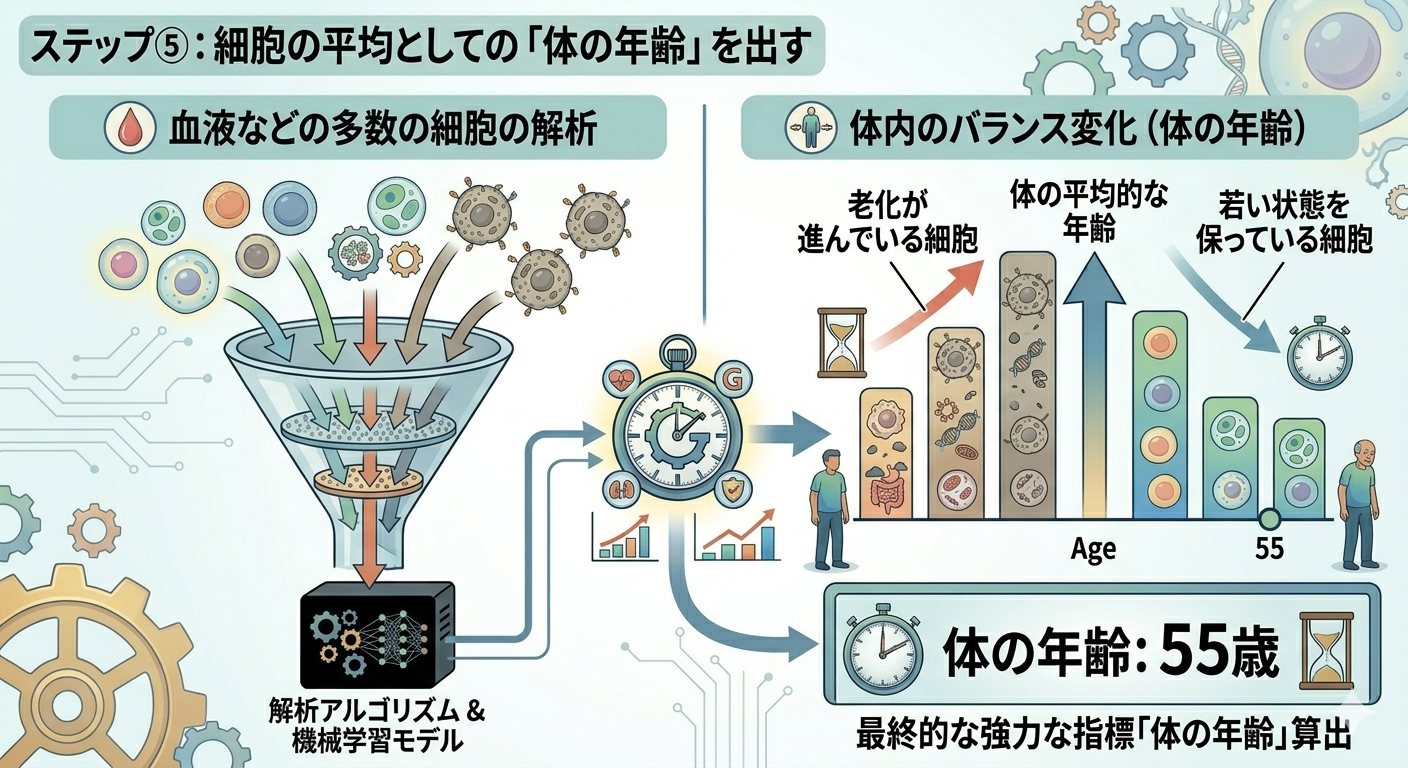
ステップ⑤:細胞の平均としての「体の年齢」を出す
実際の検査では、血液などから得られる多数の細胞をまとめて解析します。
そのため、得られる結果は「個々の細胞の年齢」ではなく「全体の平均的な年齢」です。
しかし重要なのは、この平均値が非常に強力な指標である点です。
なぜなら、
- 老化が進んでいる細胞が増える
- 若い状態を保っている細胞が減る
といった“体内のバランス変化”を反映しているからです。
この技術の本質:老化は“パターン認識”で測られる
DNAメチル化時計の本質は、単一の原因を測っているわけではないことにあります。
それはむしろ、
「無数の微細な変化のパターン」から老化を読み解く技術です。
例えるなら、
- 一本の木を見るのではなく
- 森全体の変化から季節を判断する
ようなものです。
この“パターン認識”という発想こそが、従来のバイオマーカーと決定的に異なる点です。
なぜこれほど精度が高いのか
エピジェネティッククロックが高精度である理由は、以下の特徴にあります。
- 複数のシグナルを統合している(単一指標ではない)
- 組織を超えて共通する老化パターンを捉えている
- 環境要因を反映する“動的な指標”である
そのため、単なる年齢推定を超えて、「健康状態そのもの」を映し出す指標となっているのです。
予測される今後の進化
現在のエピジェネティッククロックは、血液などから得られた多数の細胞をまとめて解析し、その平均的な状態から生物学的年齢を導き出しています。
いわば「体全体の傾向」を一つの数値として捉えている段階です。
しかし今後は、この解析の解像度が大きく変わっていくと考えられています。
細胞をひとまとめにして評価するのではなく、一つひとつの細胞を個別に解析する技術が進み、さらに時間の経過に沿ってその変化を追跡することも可能になっていきます。
そして、それらのデータをもとに、個人ごとに最適化されたエピジェネティッククロックが構築されるようになります。
こうした進化によって、単に「あなたの体は何歳か」を知るだけでなく、「体の中のどの細胞が、どのくらいのスピードで老化しているのか」まで具体的に把握できる時代が現実のものとなりつつあるのです。
細胞レベルで見た老化の正体
──老化とは「劣化」ではなく「情報の乱れ」である
エピジェネティッククロックが捉えている老化は、単に細胞が傷んでいくという単純な現象ではありません。
その本質は、むしろ「細胞のアイデンティティが徐々に失われていくプロセス」にあります。
本来、細胞はそれぞれ明確な役割を持ち、「何をするべきか」を正確に理解しています。しかし老化が進むにつれて、その設計情報に微細なズレが生じ、次第に本来の機能から逸脱していきます。
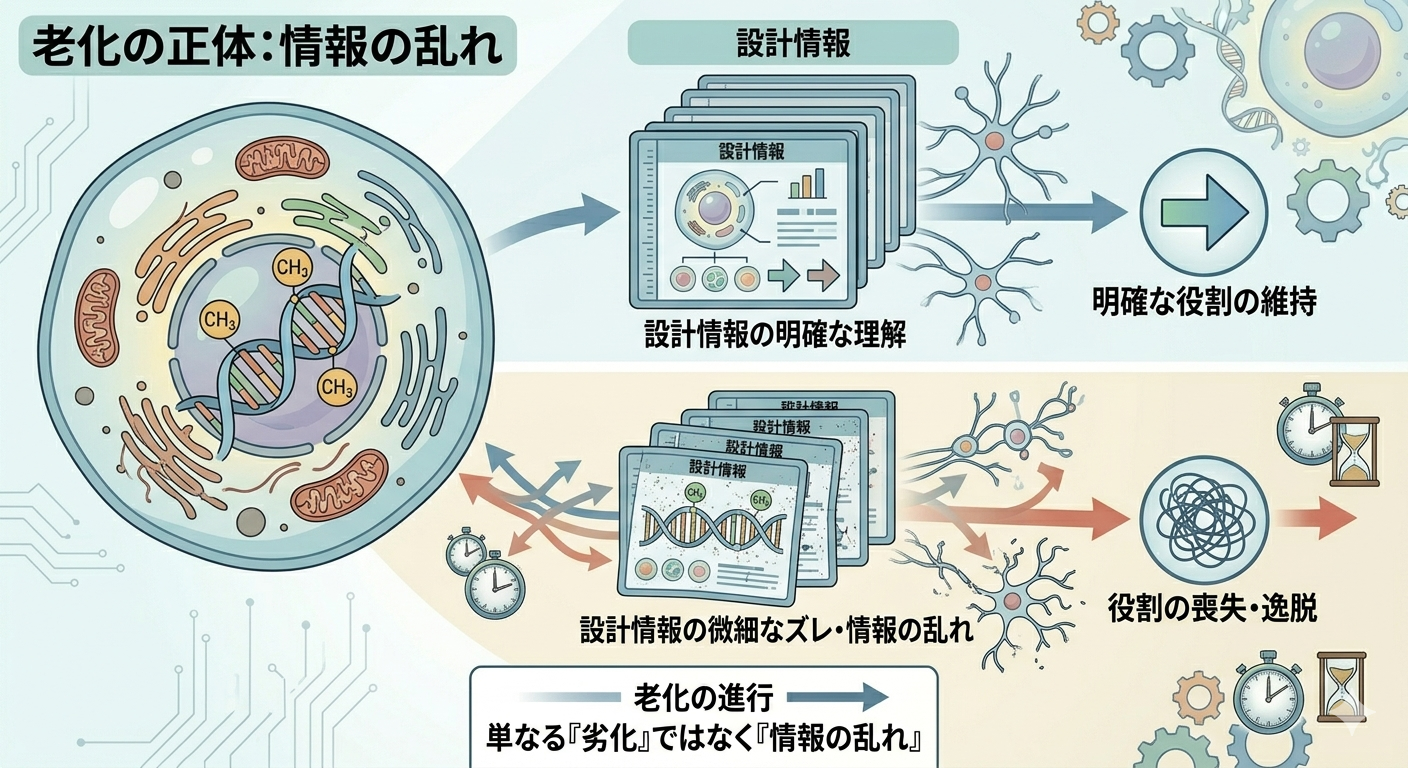
老化に伴って起きる変化
この過程では、まず遺伝子発現の精度が低下し、必要なタイミングで必要な遺伝子が適切に働かなくなります。すると細胞の役割そのものが曖昧になり、本来の機能を十分に果たせなくなります。
さらに、細胞内の情報処理には“ノイズ”が増え、正確な制御が難しくなっていきます。その結果として起きているのが、「細胞が自分の役割を見失う」という状態です。
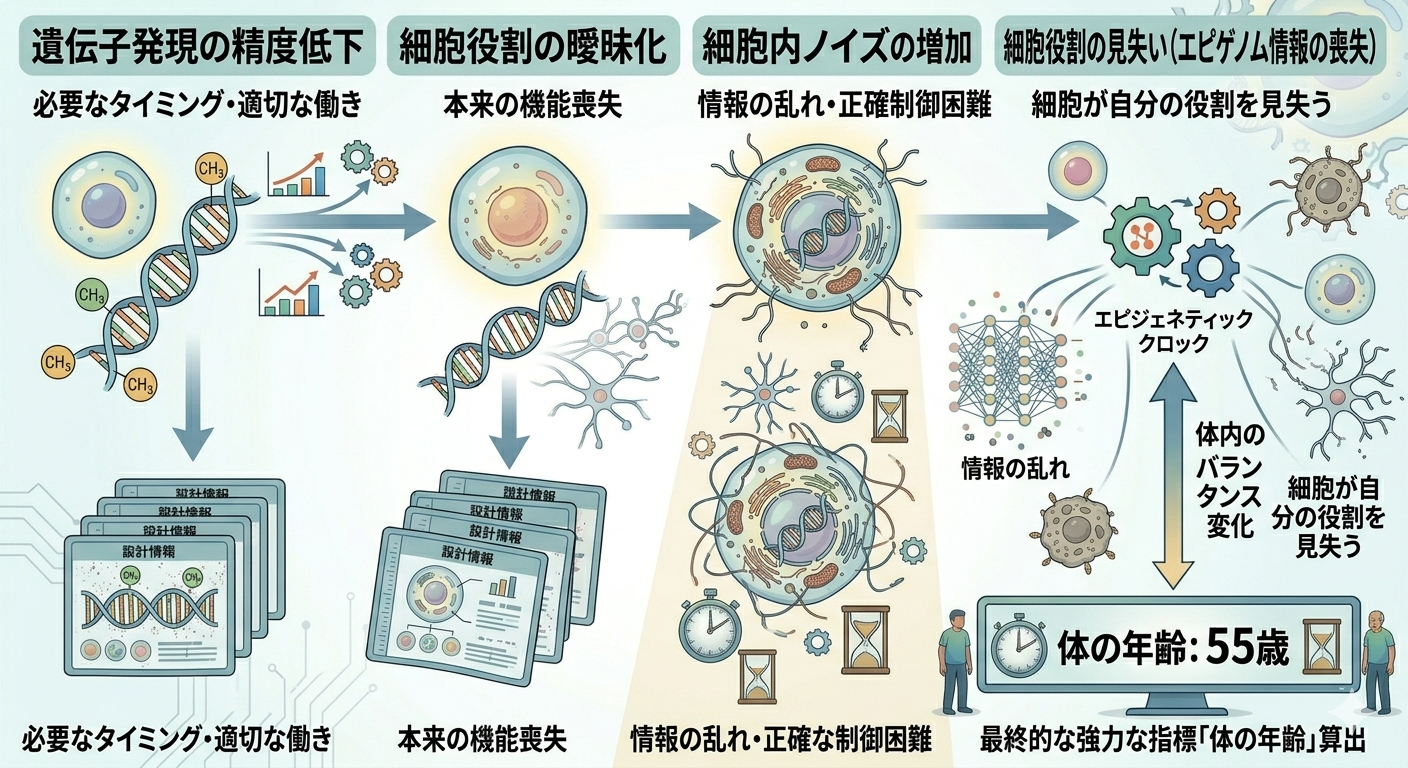
これは単なる劣化ではなく、エピゲノム情報の喪失と呼ばれる現象であり、エピジェネティッククロックはこの変化を鋭敏に捉えています。
エピジェネティッククロックが捉える“老化の軸”
興味深いのは、エピジェネティッククロックが従来の老化指標とは異なる視点から老化を捉えている点です。
この指標は、細胞がどのように栄養を感知し、どのようにエネルギーを産生し、どのように再生能力を維持しているかといった、生命活動の根幹に関わるプロセスと深く結びついています。
例えば、mTORを中心とした栄養感知システムやミトコンドリアの機能、さらには幹細胞の維持能力や細胞同士のコミュニケーションの状態などが、エピジェネティックな変化と密接に関連しています。
一方で、一般的に老化の指標として知られているテロメアの短縮やゲノムの不安定性、いわゆる細胞老化といった現象とは、必ずしも一致しません。
これはつまり、エピジェネティッククロックが従来とは異なる“もう一つの老化の軸”を見ていることを意味しています。
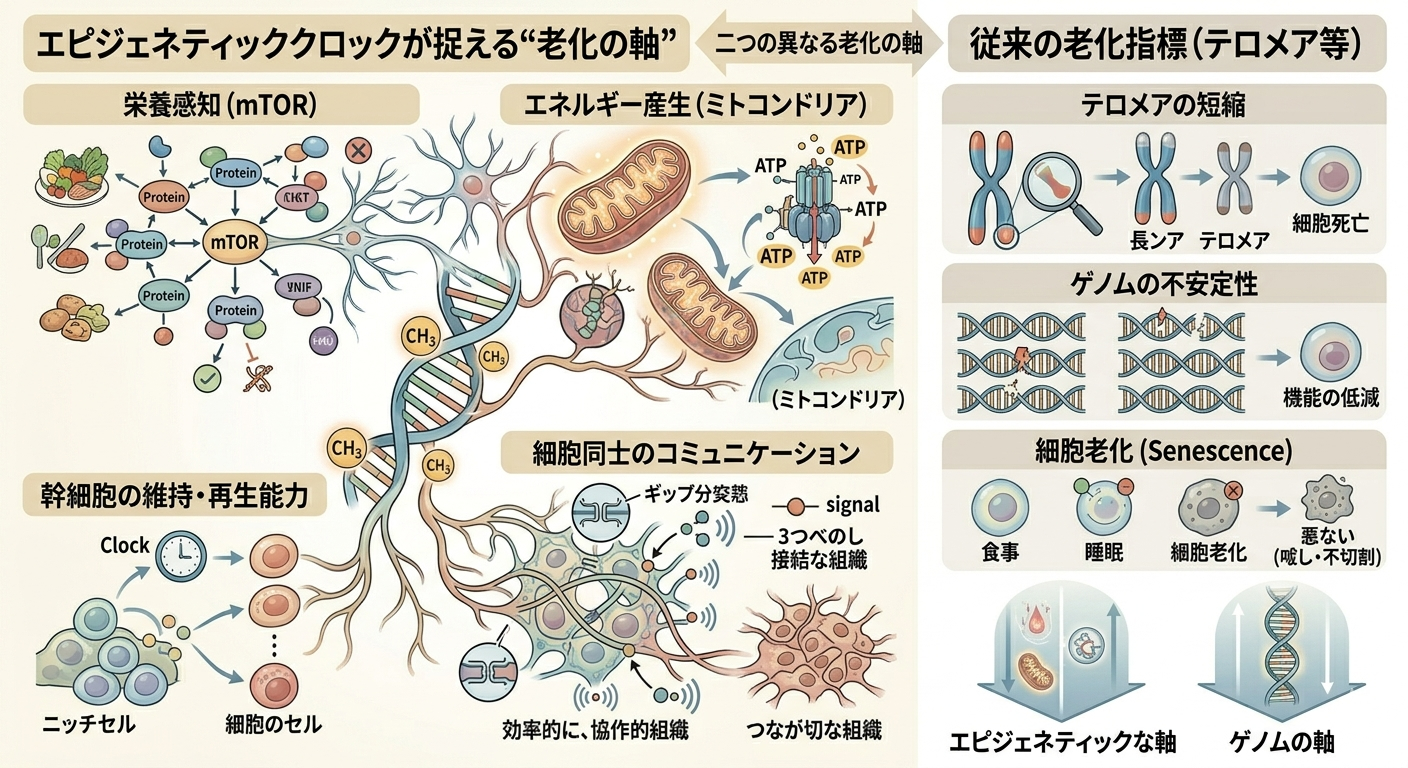
なぜ環境が老化を左右するのか
──老化は「生き方の履歴」である
DNAメチル化は固定されたものではなく、環境によって変化するという特徴を持っています。
そのため、エピジェネティッククロックは単なる体内の状態ではなく、「これまでどのように生きてきたか」という履歴そのものを反映します。
例えば、栄養状態の偏りや慢性的なストレス、社会的な環境、さらには感染症や炎症といった要因は、いずれもエピジェネティックな変化を通じて老化のスピードに影響を与えることが分かっています。
つまり老化とは、遺伝子だけで決まるものではなく、生物学と環境の相互作用によって形づくられる現象なのです。
若返りは可能なのか
──「リセット」という新しい発想
ここで注目されるのが、エピジェネティック年齢は“固定されたものではない”という事実です。
実際に、胚性幹細胞やiPS細胞といった未分化の細胞は、エピジェネティッククロック上では完全に若い状態を示します。
これは、細胞が一度「初期化」されることで、エピゲノムの状態がリセットされることを意味しています。
この現象は、理論上、細胞が若さを取り戻すことが可能であることを示唆しています。
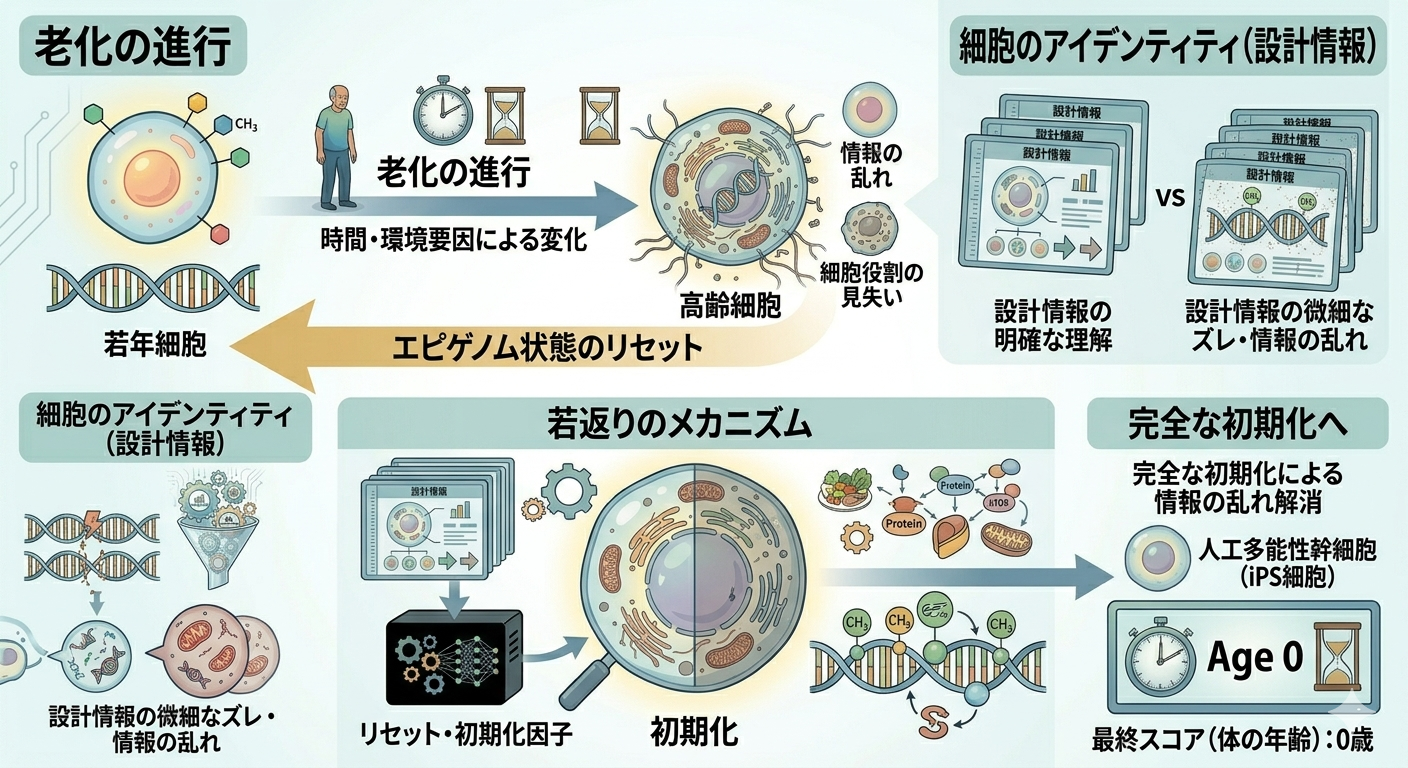
老化治療への応用
こうした知見をもとに、細胞の状態を若返らせる「リプログラミング」という技術が研究されています。これは老化そのものに介入するアプローチとして非常に有望視されていますが、一方で制御の難しさやがん化のリスクといった課題も存在しており、臨床応用はまだ発展途上の段階にあります。
現時点での実用性
──すでに始まっている“老化の可視化”
現在、エピジェネティッククロックはすでに実用化されており、少量の採血によって生物学的年齢や老化の進行速度、さらには実年齢との差であるエイジギャップを測定することが可能になっています。
日本においても「エピクロック®」などの検査が提供されており、抗老化医療の現場で活用が進んでいます。

この技術の本質的な価値は、老化という曖昧な現象を「数値」として捉えられる点にあります。
生活習慣の改善や治療介入の効果を客観的に評価できるため、予防医療や健康管理の意思決定において重要な役割を果たし始めています。
限界と課題
一方で、この技術はまだ発展途上でもあります。測定の精度や再現性には議論の余地があり、同一サンプル内でもばらつきが生じることがあります。
また、機械学習に依存しているため、結果の算出過程がブラックボックス化している点も課題の一つです。
そのため現時点では、疾患の診断を直接行うツールとしてではなく、あくまでリスク評価や変化の指標として活用されている段階にあります。
未来:老化は「管理する対象」へ
エピジェネティッククロックの登場によって、老化は初めて“測定できる現象”となりました。
これは医療にとって大きな転換点です。
今後は、より高精度な解析技術の発展により、単一細胞レベルでの老化測定や、個人ごとに最適化された評価指標が実現していくと考えられています。
また、創薬の分野においても応用が進み、老化そのものを標的とした治療戦略が現実のものとなる可能性があります。
将来的には、規制の枠組みの中でも「老化」が正式な治療対象として位置づけられる時代が訪れるかもしれません。
まとめ
──老化は“時間”ではなく“情報”で進む
老化とは、単なる時間の経過ではなく、細胞内の情報が少しずつ乱れ、再編成されていくプロセスです。
エピジェネティッククロックは、その目に見えない変化を可視化し、私たちに新しい視点をもたらしました。
それは単なる検査ではなく、自分の身体がどのように変化しているのかを理解し、未来をどう設計するかを考えるための「羅針盤」です。
これからの抗老化は、若さを保つことを目的とするのではなく、老化を理解し、主体的にマネジメントする時代へと移行していきます。
そしてその中心にあるのが、DNAが刻むもう一つの時間——エピジェネティッククロックなのです。
この記事を書いた人
1978年生まれ、京都府出身。看護師として京都市内の病院に8年間勤務後、上京。東京都内の総合病院にてICU(集中治療室)、NICU(新生児集中治療室)、手術室での高度急性期医療に従事。看護師プリセプターとして後進の育成にも尽力する。
臨床現場での経験から、既存の制度では対応困難なニーズを痛感し、24時間対応保育所や自費訪問看護ステーションを自ら立ち上げた起業家としての側面も持つ。
現在は、訪問看護の発展を支援する総合Webメディア「いろいろナース」および、抗老化とロンジェビティ(長寿科学)の実践をガイドする「こもれび抗老化ステーション」の編集長を務める。医療現場のリアルな知見と最新のロンジェビティ理論を融合させ、日本人の健康寿命延伸に寄与する情報発信を行っている。


